题目内容
【题目】美国亚利桑那州大学和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为2H2O(g) ![]() 2H2(g)+O2(g)。有关该反应的说法错误的是( )
2H2(g)+O2(g)。有关该反应的说法错误的是( )
A.没有人造树叶和太阳能的作用该反应不能自发进行
B.该反应最终是将太阳能转化为电能
C.该反应为充分利用太阳能开辟了广阔前景
D.氢能是理想的绿色能源
【答案】B
【解析】
A. 自然条件下,H2O(g)无法转化为H2和O2,因此在没有人造树叶和太阳能的作用下,该反应不能自发进行,故A正确;
B. 该反应过程中,没有产生电能,因此不存在太阳能和电能的转化,故B错误;
C. 该反应利用了太阳能,实现了太阳能的转化,为充分利用太阳能开辟了广阔前景,故C正确;
D. H2燃烧生成H2O,H2O分解产生H2,可实现循环利用,且不会造成污染,因此氢能是理想的绿色能源,故D正确。
综上所述,答案为B。

【题目】重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO、Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
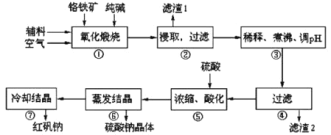
①中涉及的主要反应有:
主反应:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是________。
(2)“③”中调节pH至4.7,目的是________。
(3)“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式:________。
,请写出该平衡转化的离子方程式:________。
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶(锥形瓶)中,加入10mL2mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol·L-1Na2S2O3标准溶液滴定(I2+2![]() =2I-+
=2I-+![]() )。
)。
①判断达到滴定终点的依据是:________;
②若实验中共用去Na2S2O3标准溶液40.00mL,所得产品的中Na2Cr2O7的纯度(设整个过程中其它杂质不参与反应)________。