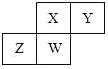��Ŀ����
����Ŀ����ͼΪԪ�����ڱ���һ���֣�����A��B��C��D��E����Ԫ�ء�����˵��������ǣ� ��

A.Ԫ��B��D��Ӧ��ٴ��ı�ʶΪ��A
B.E�ĺ���������ǿ��D�ĺ�����
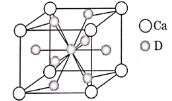
C.�۵㣺D�������C��������
D.AE3����������ԭ�Ӷ�����8�����ȶ��ṹ
���𰸡�B
��������
�����ڱ�Ԫ��B��D��Ӧ��ٴ��ı�ʶΪ��A��AΪNԪ�أ�BΪOԪ�أ�CΪSiԪ�أ�DΪSԪ�أ�EΪClԪ�ء�
A��O��S���ڢ�A����A��ȷ��
B��E������������Ӧ�ĺ���������ǿ��D������������Ӧ�ĺ����ᣬ�ͼ�̬�ĺ���������Բ�ȷ������B����
C��SO2���ڷ��Ӿ��壬SiO2����ԭ�Ӿ��壬�۵㣺D��������SO2��C��������SiO2����C��ȷ��
D��Clԭ�������7���ӣ���һ�������ӣ�Nԭ�������5�����ӣ���3��ĩ�ɶԵ��ӣ��ֱ����ȵ�һ���������γ��������ۼ���NCl3����������ԭ�Ӷ�����8�����ȶ��ṹ����D��ȷ��
��ѡB��

��ϰ��ϵ�д�
�����Ŀ