题目内容
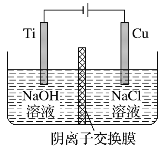
【题目】用阴离子交换膜控制电解液中OH-的浓度制备纳米Cu2O,反应为2Cu+H2O![]() Cu2O+H2↑,装置如图,下列说法中正确的是
Cu2O+H2↑,装置如图,下列说法中正确的是
A. 电解时Cl-通过交换膜向Ti极移动
B. 阳极发生的反应为:2Cu -2e- +2OH- = Cu2O+H2O
C. 阴极OH-放电,有O2生成
D. Ti电极和Cu电极生成物物质的量之比为2∶1
【答案】B
【解析】
根据装置图和电解总反应分析,Cu极为阳极,Cu极电极反应式为2Cu-2e-+2OH-=Cu2O+H2O;Ti极为阴极,Ti极电极反应式为2H2O+2e-=H2↑+2OH-;电解池中阴离子通过阴离子交换膜向阳极移动;据此分析作答。
Cu极与外加电源的正极相连,Cu极为阳极,Ti极与外加电源的负极相连,Ti极为阴极;
A项,电解时阴离子向阳极移动,OH-通过阴离子交换膜向Cu极移动,A项错误;
B项,Cu极为阳极,阳极电极反应式为2Cu-2e-+2OH-=Cu2O+H2O,B项正确;
C项,Ti极为阴极,阴极电极反应式为2H2O+2e-=H2↑+2OH-,阴极有H2生成,C项错误;
D项,根据电极反应式和阴、阳极得失电子相等,Ti极生成的H2和Cu极生成的Cu2O物质的量之比为1:1,D项错误;
答案选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目