题目内容
在一定温度下,A2、B2、AB三种分子有如下反应发生:A2(g)+B2(g)?2AB(g),该反应达到平衡时的标志是( )
| A、容器内压强不随时间变化 |
| B、AB的生成速率与消耗速率相等 |
| C、A2、B2的浓度和AB的浓度相等 |
| D、A2、B2、AB的分子数之比为1:1:2 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、容器内压强,始终不变,故A错误;
B、AB的生成速率与消耗速率相等,正逆反应速率相等,故B正确;
C、A2、B2的浓度和AB的浓度相等,而不是不变,故C错误;
D、当体系达平衡状态时,A2、B2、AB的分子数之比可能为1:1:2,也可能不是1:1:2,与各物质的初始浓度及转化率有关,故D错误;
故选B.
B、AB的生成速率与消耗速率相等,正逆反应速率相等,故B正确;
C、A2、B2的浓度和AB的浓度相等,而不是不变,故C错误;
D、当体系达平衡状态时,A2、B2、AB的分子数之比可能为1:1:2,也可能不是1:1:2,与各物质的初始浓度及转化率有关,故D错误;
故选B.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
在100℃时,NaCl溶液中c(H+)=1×10-6mol?L-1.下列说法中正确的是( )
| A、该NaCl溶液显酸性 |
| B、该NaCl溶液显中性 |
| C、该NaCl溶液中Kw=c(H+)?c(OH-)=1×10-14 |
| D、该NaCl溶液中Kw=c(H+)?c(OH-)=1×10-12 |
某离子化合物的晶胞结构如图所示,则该晶体中X、Y的离子个数之比是( )
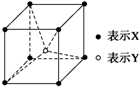

| A、4:1 | B、1:1 |
| C、2:1 | D、1:2 |
化学平衡移动的原理在现实生活和生产等社会的许多方面有着广泛的应用.下列应用中涉及的有关原理与化学平衡移动无关的是( )
| A、用酸碱指示剂测定溶液的酸碱性 |
| B、将煤气中毒病人置于高压氧仓中治疗 |
| C、硫酸工业中将硫铁矿粉碎后煅烧 |
| D、交警常用酒精测试仪检查司机是否酒后驾车 |
下列分子中,其中心原子杂化轨道类型相同的是( )
| A、H2O与NH3 |
| B、CO2与SO2 |
| C、BeCl2与BF3 |
| D、C2H2与C2H4 |
二氧化硅的化学性质很不活泼,几乎所有的酸都不与其反应,但有一种酸能够和二氧化硅发生反应,这种酸是( )
| A、浓盐酸 | B、硫酸 |
| C、硝酸 | D、氢氟酸 |
共价键、离子键和分子间作用力是粒子之间的三种作用力.下列晶体:①NaOH ②SiO2 ③石墨④NaCl ⑤干冰中,含有两种作用力的是( )
| A、①②③ | B、①③⑤ |
| C、②④⑤ | D、②③④ |
下列关于元素周期表和元素周期律的说法错误的是( )
| A、F、Cl、Br元素的原子核外电子层数随着核电荷数的增加而增多 |
| B、L层电子数为奇数的所有元素所在族的序数与该元素原子的L层电子数相等 |
| C、因为K比Na容易失去电子,所以K比Na的还原性强 |
| D、周期表中元素最多的族是Ⅷ族,过渡元素全部都为金属元素 |
可逆反应2NO2(g)?N2O4(g)△H<0,试根据下列图象,判断t2,t3,t4时刻采取的措施是( )


| A、加入NO2、升高温度、增大压强 |
| B、加入N2O4、减小压强、加催化剂 |
| C、加入NO2、降低温度、减小压强 |
| D、加入N2O4、降低温度、加催化剂 |