题目内容
12.不可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )| A. | 一个N≡N断裂的同时,有3个H-H键断裂 | |
| B. | 保持其它条件不变时,体系压强不再改变 | |
| C. | 恒温恒容时,密度保持不变 | |
| D. | 正反应速率v(H2)=0.6mol/L•min,逆反应速率v(NH3)=0.4mol/L•min |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、一个N≡N断裂的同时,有3个H-H键断裂,都体现的正反应方向,故A错误;
B、随着反应的进行体系压强逐渐减小,容器内压强保持不变说明达平衡状态,故B正确;
C、恒温恒容时,密度始终保持不变,故C错误;
D、正反应速率v(H2)=0.6mol/L•min,逆反应速率v(NH3)=0.4mol/L•min,所以2v正(H2)=3v正(NH3)=3v逆(NH3),故D正确;
故选AC.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.已知链式炔碳C300经过适当处理可得含多个-C≡C-(不含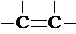 )的链状化合物C300H298,则含-C≡C-的个数为( )
)的链状化合物C300H298,则含-C≡C-的个数为( )
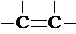 )的链状化合物C300H298,则含-C≡C-的个数为( )
)的链状化合物C300H298,则含-C≡C-的个数为( )| A. | 70 | B. | 72 | C. | 74 | D. | 76 |
1.分子式为C6H12O2的有机物A,有香味,不能使紫色石蕊试液变红.A在酸性条件下水解生成有机物B和甲醇.则A可能的结构有( )
| A. | 1种 | B. | 3种 | C. | 4种 | D. | 多于4种 |
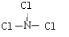 ;由A、B、D三种元素组成的18电子微粒的电子式为
;由A、B、D三种元素组成的18电子微粒的电子式为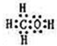
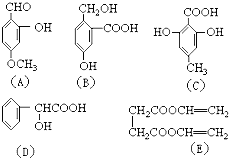 下列有机物中,有多个官能团:可以看作醇类的是
下列有机物中,有多个官能团:可以看作醇类的是
 ,五种元素中,电负性最大的元素是F,能形成强含氧酸的元素是N、S,第I电离能最小的是Al.
,五种元素中,电负性最大的元素是F,能形成强含氧酸的元素是N、S,第I电离能最小的是Al.