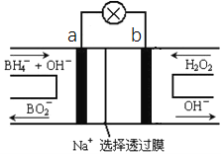
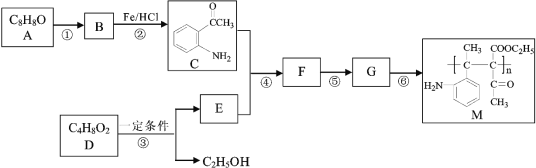
题目内容
【题目】某研究性学习小组为了解有机物A的性质,对A的结构进行了如下实验。
实验一:通过质谱分析仪分析得知有机物A的相对分子质量为90。
实验二:用红外光谱分析发现有机物A中含有—COOH和 —OH。
实验三:取1.8g有机物A完全燃烧后,测得生成物为2.64gCO2和1.08gH2O。
实验四:经核磁共振检测发现有机物A的谱图中H原子峰值比为3:1:1:1。
(1)有机物A的结构简式为_______。
(2)有机物A在一定条件下可以发生的反应有_______。
a.消去反应 b.取代反应 c.聚合反应 d.加成反应 e.氧化反应
(3)有机物A在浓硫酸作用下可生成多种产物。其中一种产物B的分子式为C3H4O2,B能和溴发生加成反应,则B的结构简式为_______。另一种产物C是一种六元环状酯,写出生成C的化学方程式:_______。
(4)写出A与足量的金属钠反应的化学方程式:_______。
【答案】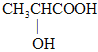 abce CH2=CHCOOH 2
abce CH2=CHCOOH 2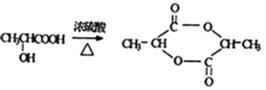 +2H2O
+2H2O 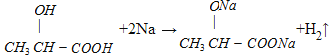
【解析】
2.64gCO2和1.08gH2O 中碳元素、氢元素的物质的量分别是![]() 、
、![]() ,根据质量守恒,1.8g有机物A中氧元素的物质的量是
,根据质量守恒,1.8g有机物A中氧元素的物质的量是![]() ,A的最简式是CH2O,A的相对分子质量是90,所以A的分子式是C3H6O3;
,A的最简式是CH2O,A的相对分子质量是90,所以A的分子式是C3H6O3;
(1) A的分子式是C3H6O3,A中含有—COOH和 —OH ,核磁共振检测发现有机物A的谱图中H原子峰值比为3:1:1:1,则A的结构简式是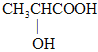 ;
;
(2) a.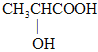 含有羟基,能发生消去反应生成CH2=CHCOOH,故选a;
含有羟基,能发生消去反应生成CH2=CHCOOH,故选a;
b.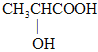 含有羟基、羧基能发生酯化反应,酯化反应属于取代反应,故选b;
含有羟基、羧基能发生酯化反应,酯化反应属于取代反应,故选b;
c.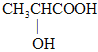 含有羟基、羧基能发生缩聚反应,故选c;
含有羟基、羧基能发生缩聚反应,故选c;
d.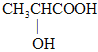 不含碳碳双键,不能发生加成反应,故不选d;
不含碳碳双键,不能发生加成反应,故不选d;
e.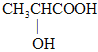 含有羟基,能发生氧化反应,故选e;
含有羟基,能发生氧化反应,故选e;
选abce;
(3) B的分子式为C3H4O2,B能和溴发生加成反应,说明B含有碳碳双键,则B的结构简式为CH2=CHCOOH;另一种产物C是一种六元环状酯,则C是 ,2分子
,2分子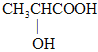 发生酯化反应生成
发生酯化反应生成 和水,反应的化学方程式是2
和水,反应的化学方程式是2 +2H2O;
+2H2O;
(4) 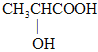 中羟基、羧基都能与钠发生置换反应放出氢气,反应的化学方程式是
中羟基、羧基都能与钠发生置换反应放出氢气,反应的化学方程式是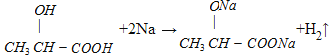 。
。