题目内容
研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法不正确的是( )
| A、羰基硫分子为非极性分子 |
B、羰基硫的电子式为: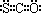 |
| C、羰基硫沸点比CO2高 |
| D、羰基硫分子中三个原子处于同一直线上 |
考点:极性分子和非极性分子,电子式
专题:化学键与晶体结构
分析:羰基硫可以看作是二氧化碳分子中的一个碳原子被硫原子取代.
A.根据极性分子中正负电荷的中心不重合,具有一定的极性;
B、根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式.
C、根据分子晶体中物质的熔沸点与相对分子质量的关系判断.
D、根据二氧化碳的结构判断羰基硫的结构.
A.根据极性分子中正负电荷的中心不重合,具有一定的极性;
B、根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式.
C、根据分子晶体中物质的熔沸点与相对分子质量的关系判断.
D、根据二氧化碳的结构判断羰基硫的结构.
解答:
解:A、二氧化碳结构对称,所以羰基硫也是直线型分子,但2个极性键的极性不等,所以中正负电荷的中心不重合,是极性分子,故A错误;
B、羰基硫中分子中所有原子的最外层都满足8电子结构,碳原子能形成4个共价键,硫原子能形成2个共价键,氧原子能形成2个共价键,所以其电子式为 ,故B正确.
,故B正确.
C、分子晶体中,一般的相对分子质量越大其熔沸点越大,羰基硫的相对分子质量大于二氧化碳的相对分子质量,所以羰基硫的熔沸点大于二氧化碳的,故C正确;
D、二氧化碳是直线型分子,羰基硫可以看作是二氧化碳分子中的一个碳原子被硫原子取代,所以羰基硫也是直线型分子,故D正确;
故选A.
B、羰基硫中分子中所有原子的最外层都满足8电子结构,碳原子能形成4个共价键,硫原子能形成2个共价键,氧原子能形成2个共价键,所以其电子式为
 ,故B正确.
,故B正确.C、分子晶体中,一般的相对分子质量越大其熔沸点越大,羰基硫的相对分子质量大于二氧化碳的相对分子质量,所以羰基硫的熔沸点大于二氧化碳的,故C正确;
D、二氧化碳是直线型分子,羰基硫可以看作是二氧化碳分子中的一个碳原子被硫原子取代,所以羰基硫也是直线型分子,故D正确;
故选A.
点评:本题考查了物质结构中的有关知识,属于信息给予题目,注意利用二氧化碳结构进行知识迁移运用.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列各组分子中,均含有非极性键且属于非极性分子的是( )
| A、Cl2 C2H4 |
| B、C2H4 CH4 |
| C、CO2 H2S |
| D、NH3 HCl |
下列化学用语及其说法正确的是( )
| A、H、D、T互为同素异形体,化学性质几乎完全相同 |
B、硫离子结构示意图: |
| C、吸氧腐蚀的正极反应式为:O2+2H2O+4e-═4OH- |
D、NaOH的电子式为: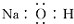 |
下列描述中正确的是( )
| A、CS2为V形分子 |
| B、NCl3的空间构型为平面三角形 |
| C、铝的第一电离能比镁的第一电离能大 |
| D、SiF4和H2O的中心原子均为sp3杂化 |
试判断C5H12O的同分异构体的种数( )
| A、8 | B、10 | C、13 | D、14 |
判断下列化合物中标出的显正价的元素正确的是( )
| A、OF2(F显正价) |
| B、CN-离子(N显正价) |
| C、NH3(H显正价) |
| D、SiC (C显正价) |
通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
| A、分子中的所有原子均达到8电子稳定结构 |
| B、分子中N-C1键键长与CCl4分子中C-Cl键键长相等 |
| C、NCl3分子是平面三角形非极性分子 |
| D、NBr3比NCl3易挥发 |
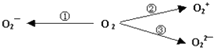 据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子
据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子