题目内容
某学生拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量而生成NaHCO3,他设计了如下实验步骤:①取25mLNaOH溶液吸收过量CO2气体,至CO2气体不再溶解;②小心煮沸溶液1~2min排除溶液中溶解的CO2气体;③在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。

(1)他能否制得较纯净的Na2CO3?________理由是_________________________________
_____________________________________________________________________________。
按他的设计,第①步实验装置如图所示:
(2)装置A使用的试剂是石灰石和盐酸溶液,可否使用纯碱代替石灰石?________________原因是____________________________________________________________________________________________。
(3)装置B使用的试剂是________________,作用是________________。
(4)有人认为验步骤②③的顺序对调,即先混合,再煮沸,更合理,你认为对吗?为什么?
解析:
(1)能 实验①生成NaHCO3,其中溶解的CO2气体煮沸时除去,在实验③NaHCO3恰好被NaOH中和完全转化成Na2CO3。 (2)不能 实验中使用的CO2的气体发生器,只适用于块状固体和液体反应,Na2CO3是粉末状固体,反应过于猛烈。 (3)NaHCO3饱和溶液 除去HCl (4)不合理;若不先驱除溶液中溶解的CO2气体,实验③加入的NaOH将有一部分消耗于与CO2气体的反应,使NaHCO3不能完全转化为Na2CO3。
|

| A、食醋 | B、花生油 | C、酱油 | D、白酒 |

 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( )
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( )
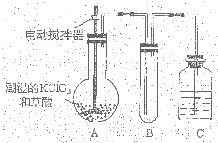 二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题:
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题: