题目内容
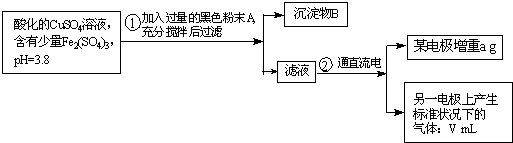
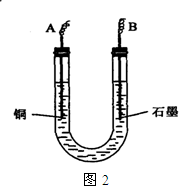
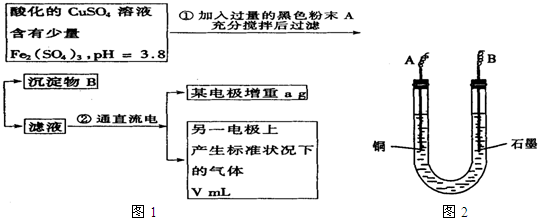
 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( )
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( )分析:X为CuO,与酸反应调节溶液pH,可促进铁离子的水解而除去杂质,反应中铜为电解池阴极,石墨为阳极,阴极反应为Cu2++2e-=Cu,阳极反应为4OH--4e-=O2↑+2H2O,根据两极转移电子数目相等计算铜的相对原子质量.
解答:解:A.铜为电解池阴极,应连接电源负极,故A错误;
B.X为CuO,与酸反应调节溶液pH,可促进铁离子的水解而除去杂质,故B错误;
C.设铜的相对原子质量为M,则n(Cu)=
mol,n(O2)=
mol,两极转移电子数目相等,则
mol×2=
mol×4,则M=
,故C错误;
D.石墨为阳极,电极上发生的反应是4OH--4e-=O2↑+2H2O,故D正确.
故选D.
B.X为CuO,与酸反应调节溶液pH,可促进铁离子的水解而除去杂质,故B错误;
C.设铜的相对原子质量为M,则n(Cu)=
| a |
| M |
| V×10-3 |
| 22.4 |
| a |
| M |
| V×10-3 |
| 22.4 |
| V×10-3 |
| 11.2a |
D.石墨为阳极,电极上发生的反应是4OH--4e-=O2↑+2H2O,故D正确.
故选D.
点评:本题考查电解原理,题目难度不大,注意根据电极增重和生成气体判断电解池的两极反应,根据两极转移电子数目相等的关系测定铜的相对原子质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )