题目内容
【题目】下面提到的问题中,与盐的水解无关的正确说法是
①明矾和FeCl3可作净水剂
②为保存FeCl3溶液,要在溶液中加少量盐酸
③AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3
④NH4Cl与ZnCl2溶液可作焊接中的除锈剂
⑤实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
⑦长期使用硫铵,土壤酸性增强;草木灰与铵态氮肥不能混合施用
A.①④⑦B.全有关C.②⑤D.③⑥
【答案】B
【解析】
①明矾和FeCl3可作净水剂的原因是铝离子、铁离子水解生成胶体具有较大的表面积,具有吸附悬浮杂质的作用,故①与盐的水解有关;②FeCl3溶液中存在水解平衡:Fe3++3H2O![]() Fe(OH)3+3H+,加入盐酸抑制铁离子的水解,故②与盐的水解有关;③氯化铝水解生成Al(OH)3和氯化氢,加热时由于氯化氢的挥发,促进AlCl3水解最终完全水解成氢氧化铝,灼烧氢氧化铝得到氧化铝,故③与盐的水解有关;④NH4+、Zn2+水解使NH4Cl、ZnCl2溶液显酸性,铁锈反应,故④与盐的水解有关;⑤碳酸根、硅酸根离子水解使溶液显碱性和玻璃中的二氧化硅反应,把玻璃瓶塞和瓶口粘结,故实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞,⑤与盐的水解有关;⑥HCO3-、Al3+发生双水解反应生成二氧化碳,故⑥与盐的水解有关;⑦铵根离子水解使硫酸铵溶液呈酸性,草木灰中的碳酸根离子水解使溶液显碱性,二者混合水解相互促进,肥效降低,故⑦与盐的水解有关;全与盐的水解有关,答案选B。
Fe(OH)3+3H+,加入盐酸抑制铁离子的水解,故②与盐的水解有关;③氯化铝水解生成Al(OH)3和氯化氢,加热时由于氯化氢的挥发,促进AlCl3水解最终完全水解成氢氧化铝,灼烧氢氧化铝得到氧化铝,故③与盐的水解有关;④NH4+、Zn2+水解使NH4Cl、ZnCl2溶液显酸性,铁锈反应,故④与盐的水解有关;⑤碳酸根、硅酸根离子水解使溶液显碱性和玻璃中的二氧化硅反应,把玻璃瓶塞和瓶口粘结,故实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞,⑤与盐的水解有关;⑥HCO3-、Al3+发生双水解反应生成二氧化碳,故⑥与盐的水解有关;⑦铵根离子水解使硫酸铵溶液呈酸性,草木灰中的碳酸根离子水解使溶液显碱性,二者混合水解相互促进,肥效降低,故⑦与盐的水解有关;全与盐的水解有关,答案选B。

 阅读快车系列答案
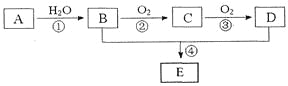
阅读快车系列答案【题目】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省 略),反应原理如下:
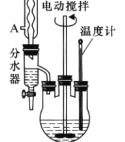
 +C2H5OH
+C2H5OH +H2O
+H2O
实验操作步骤:
向三颈烧瓶内加入12.2g 苯甲酸、25mL乙醇、20mL 苯及4mL浓硫酸,摇匀,加入沸石。
①装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒 中,继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
②将反应液倒入盛有80mL冷水的烧瓶中,在搅拌下分批加入碳酸钠粉末溶液至溶液无二氧化 碳逸出,用 pH 试纸检验至中性。
③用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水CaCl2干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接受210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,易溶于乙醇、乙醚 |
乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
(1)反应装置中分水器上方的仪器名称是_______,其作用是______。
(2)步骤①中加入浓硫酸的作用是______,步骤②中电动搅拌棒的作用是_______。
(3)步骤②中使用分水器除水的目的是______。
(4)步骤③中加入碳酸钠的目的是______。
(5)有机层从分液漏斗的_______(选填“上口倒出”或“下口放出”span>)
(6)本实验所得到的苯甲酸乙酯的产率是_______。