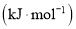题目内容
【题目】硅烷是一种无色、与空气反应并会引起窒息的气体.其分子结构和![]() 相似,但
相似,但![]() 键键能比
键键能比![]() 键键能低。下列判断错误的是
键键能低。下列判断错误的是
A.![]() 分子呈正四面体形
分子呈正四面体形
B.![]() 分子是非极性分子
分子是非极性分子
C.因为![]() 键键能比
键键能比![]() 键键能低,所以
键键能低,所以![]() 沸点低于
沸点低于![]() 沸点
沸点
D.![]() 分子稳定性低于
分子稳定性低于![]() 分子,因为
分子,因为![]() 键键能高
键键能高
【答案】C
【解析】
根据题中硅烷分子结构和![]() 相似可知,本题考查硅烷分子结构特点,运用硅烷分子结构和
相似可知,本题考查硅烷分子结构特点,运用硅烷分子结构和![]() 相似分析。
相似分析。
A.甲烷分子为正四面体构型,![]() 的分子结构与
的分子结构与![]() 类似,因此
类似,因此![]() 具有正四面体的构型,故A正确;
具有正四面体的构型,故A正确;
B.![]() 正四面体的构型,正负电荷中心对称是正四面体结构,所以是非极性分子,故B正确;
正四面体的构型,正负电荷中心对称是正四面体结构,所以是非极性分子,故B正确;
C.结构相似的分子晶体,相对分子量越大沸点越高,所以![]() 沸点高于
沸点高于![]() 沸点,故C错误;
沸点,故C错误;
D.中心元素的非金属性越强对应氢化物越稳定,因为碳的非金属性强于硅,则![]() 键键能高,所以
键键能高,所以![]() 分子稳定,故D正确;
分子稳定,故D正确;
答案选C。

练习册系列答案
相关题目
【题目】下面两表分别列出了CO和![]() 的某些性质及相关键能,有关说法不正确的是
的某些性质及相关键能,有关说法不正确的是
表1:
分子 | 熔点 | 沸点 | 常温时在水 中溶解度 |
CO |
|
|
|
|
|
|
|
表2:
CO |
|
|
|
键能 |
|
| |
|
|
|
|
键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]()
C.由表1可知,CO的熔沸点高于![]() ,是因为CO分子间作用力大于
,是因为CO分子间作用力大于![]()
D.由表1可知,室温时,CO在水中的溶解性大于![]() ,是因为CO分子有弱极性
,是因为CO分子有弱极性
【题目】CO和![]() 的某些性质及相关键能如下表所示,下列说法不正确的是
的某些性质及相关键能如下表所示,下列说法不正确的是
表一
分子 | 熔点 | 沸点 | 常温时在水中的溶解度 |
CO |
|
|
|
|
|
|
|
表二
碳氮键 |
|
|
|
键能 |
|
|
|
氮氮键 |
|
|
|
键键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]() ,因为
,因为![]() 的键能大于
的键能大于![]()
C.由表1可知,CO的熔沸点高于![]() ,因为CO分子间作用力大于
,因为CO分子间作用力大于![]()
D.由表1可知,室温时CO在水中的溶解度大于![]() ,因为CO是极性分子
,因为CO是极性分子