题目内容
已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径: A>B>D>C | B.原子序数: d>c>b>a |
| C.离子半径: C>D>B>A | D.单质的还原性: A>B>D>C |
C
试题分析:aA2+、bB+、cC2-、dD-都具有相同的电子层结构,说明a、b的电子层比c、d的电子层数多,原子半径应该是B > A > C > D;原子序数是a>b>d>c;离子半径中C>D>B>A。单质的还原性应该是A>B>D>C。
点评:本题中微粒半径的比较中当电子层数相同时,核电荷数越高半径反而越小,而对于核电荷数相等的离子来说,电荷数越高,半径反而越小。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
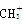 、—CH3、
、—CH3、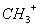 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________
 Cl ③白磷 ④氯气 ⑤红磷
Cl ③白磷 ④氯气 ⑤红磷  Cl ⑦正丁烷 ⑧异丁烷
Cl ⑦正丁烷 ⑧异丁烷