题目内容
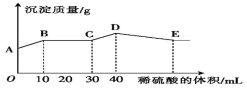
【题目】已知NO2和N2O4可以相互转化:2NO2(g) ![]() N2O4(g)△H<0,现将一定量NO2和N2O4的混合气体,通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如右图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
N2O4(g)△H<0,现将一定量NO2和N2O4的混合气体,通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如右图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是

A.如混合气体的压强不变,说明反应已达化学平衡状态
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b点
C.25~30 min内用N2O4表示的平均化学反应速率是0.04 molL-1min-1
D.反应进行至25 min时,曲线发生变化的原因是增加N2O4浓度
【答案】D
【解析】
试题分析:由图可知10-25min平衡状态时,X表示的生成物的浓度变化量为(0.6-0.2)mol/L=0.4mol/L,Y表示的反应物的浓度变化量为(0.6-0.4)mol/L=0.2mol/L,X表示的生成物的浓度变化量是Y表示的反应物的浓度变化量的2倍,所以X表示NO2浓度随时间的变化曲线,Y表示N2O4浓度随时间的变化曲线。A、该反应酯化反应为气体物质的量减少的反应,容器体积不变,随反应进行体系压强降低,压强不变,说明反应已达化学平衡状态,故A正确;B、由图可知,10-25min及35min之后X、Y的物质的量不发生变化,则相应时间段内的点处于化学平衡状态,即b处于化学平衡状态,故B正确;C、由图象可知,25~30 min内用N2O4的浓度变化量为(0.6-0.4)mol/L=0.2mol/L,所以v(N2O4)=![]() =0.04mol/(Lmin),故C正确;D、25min时,X的浓度增大,Y的浓度不变,只能是增大X的浓度,所以曲线发生变化的原因是增加NO2浓度,故D错误;故选D。
=0.04mol/(Lmin),故C正确;D、25min时,X的浓度增大,Y的浓度不变,只能是增大X的浓度,所以曲线发生变化的原因是增加NO2浓度,故D错误;故选D。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目