题目内容
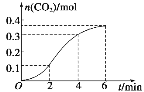
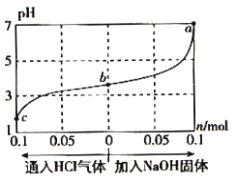
【题目】在25℃时,将1.0Lc mol·L-1 CH3COOH溶液与0.1mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述错误的是( )
A.水的电离程度:a>b>c
B.b点对应的混合溶液中:c(Na+)<c(CH3COO-)
C.c点对应的混合溶液中:c(CH3COOH)>c(Na+)>c(OH-)
D.该温度下,a、b、c三点CH3COOH的电离平衡常数均为![]()
【答案】D
【解析】
根据图示可知,原混合液显酸性,则为醋酸与醋酸钠的混合液,a点加入0.10molNaOH固体,pH=7,说明原溶液中CH3COOH的物质的量稍大于0.2mol。酸或碱抑制水的电离,含弱酸根离子的盐促进水的电离,酸或碱的浓度越大,抑制水电离程度越大。
A.1.0Lcmol·L-1 CH3COOH溶液与0.1molNaOH固体混合,发生的反应为:CH3COOH+NaOH=CH3COONa+H2O,反应后的溶液是CH3COOH和CH3COONa的混合溶液,其中CH3COONa的水解能够促进水的电离,而CH3COOH的电离会抑制水的电离。若向该混合溶液中通入HCl,b→c发生的反应为:CH3COONa+HCl=CH3COOH+NaCl,CH3COONa减少,CH3COOH增多,水的电离程度减小;若向该混合溶液中加入NaOH固体,b→a发生的反应是:CH3COOH+NaOH=CH3COONa+H2O,CH3COONa增多,CH3COOH减少,水的电离会逐渐增大,因此水的电离程度:a>b>c,故A正确;
B. b点对应的混合溶液呈酸性,c(H+)>c(OH-),则此时溶质为CH3COOH和CH3COONa,结合电荷守恒,所以c(Na+)<c(CH3COO-),故B正确;
C. c点对于的溶液是通入0.1molHCl的溶液,相当于HCl中和氢氧化钠,所以c点溶液相当于原CH3COOH溶液和0.1molNaCl固体的混合液,醋酸浓度大于0.2mol/L,所以c(CH3COOH)>c(Na+)>c(OH-),故C正确;
D.该温度下,CH3COOH的电离平衡常数![]() ,a点对于溶液中pH=7,c(Na+)=c(CH3COO-)=0.2mol/L,c(H+)=c(OH-)=10-7mol/L,则溶液中c(CH3COOH)=(c-0.2)mol/L,带入公式得
,a点对于溶液中pH=7,c(Na+)=c(CH3COO-)=0.2mol/L,c(H+)=c(OH-)=10-7mol/L,则溶液中c(CH3COOH)=(c-0.2)mol/L,带入公式得![]() ,故D错误。
,故D错误。