题目内容
草酸(H2C2O4)是二元弱酸,草酸氢钠溶液显酸性。常温下向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH) = 0时,c(H+)=1×10—2mol/L |
| B.V(NaOH) <10mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4- ) |
| C.V(NaOH) =" 10" mL时,c(H+) = 1×10—7 mol/L |
| D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4- ) |
BD
试题分析:草酸(H2C2O4)是二元弱酸,草酸氢钠溶液显酸性,这说明在草酸氢钠溶液HC2O4―的电离程度大于HC2O4―的水解程度,A不正确,c(H+)<1×10—2mol/L;V(NaOH)<10mL时,说明氢氧化钠是不足的,生成草酸钠的同时,草酸氢钠是过量的,则根据电荷守恒可知c(Na+)+c(H+)=2c(C2O42-)+c(HC2O4- )+c(OH-)。由于此时溶液可能是显中性,则c(H+)=c(OH-),所以c(Na+)=2c(C2O42-)+c(HC2O4- ),B正确;V(NaOH) =" 10" mL时,恰好反应生成草酸钠,C2O42-水解溶液显碱性,c(H+)<1×10—7 mol/L,C不正确;V(NaOH)>10 mL时,氢氧化钠是过量的,溶液存在氢氧化钠和草酸钠的混合物,所以选项D是正确的,答案选BD。
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求。本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合题意灵活运用即可。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


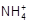 )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)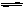 CO32—+H3O+
CO32—+H3O+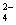 )+ c(HC2O
)+ c(HC2O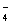 )
)