题目内容
【题目】下图是8种有机化合物的转换关系:
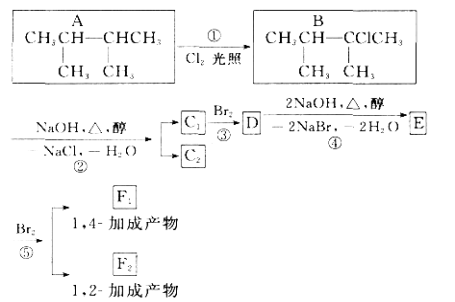
请回答下列问题:
(1)上述框图中,①是________反应,③是________反应(填反应类型)。
(2)化合物E是重要的工业原料,写出由D生成E的化学方程式:_______________________________________________________________。
(3) C 1的结构简式是______________________;F 1的结构简式是_____________________________。
(4) 上述8种化合物中,属于二烯烃的是_____________。
【答案】(1)取代;加成;(2) +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O;
+2NaBr+2H2O;
(3)![]() ;
; ;(4)E;
;(4)E;
【解析】
试题分析:上述框图中,①是A中碳原子上的氢原子在光照条件下被氯气中的氯原子取代,所以①发生的是取代反应,反应②是B在氢氧化钠的醇溶液中加热发生消去反应生成2,3-二甲基-2-丁烯或者2,3-二甲基-1-丁烯,再根据反应⑤,E和溴单质发生1,2加成得到F2,发生1,4加成得到F1,说明E是共轭二烯进一步推出,C1是![]() ,C2是2,3-二甲基-1-丁烯,(1) ①是取代反应,③是加成反应,答案为:取代;加成;(2)D是
,C2是2,3-二甲基-1-丁烯,(1) ①是取代反应,③是加成反应,答案为:取代;加成;(2)D是 ,D到E发生的是消去反应,生成的E是
,D到E发生的是消去反应,生成的E是![]() ,发生的反应为:
,发生的反应为:  +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,答案为:
+2NaBr+2H2O,答案为:  +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O;(3)C1是
+2NaBr+2H2O;(3)C1是![]() ,E是
,E是![]() 和溴单质发生1,4加成得到F1,F1是
和溴单质发生1,4加成得到F1,F1是 ,答案为:
,答案为:![]() ;
; ;(4)属于二烯烃的是E,答案为:E。
;(4)属于二烯烃的是E,答案为:E。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目