题目内容
15.已知漂白粉与浓盐酸反应产生氯气.某同学试图测定氯气的体积并验证干燥纯净的氯气无漂白性,现有如图装置,请回答: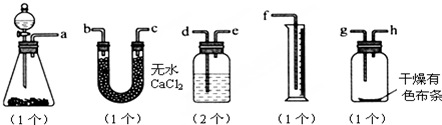
(1)请用字母填写装置的连接顺序:
a接d、e接b或c、c或b接g、h接e、d接f
( 2 )制氯气装置中滴加液体试剂的仪器名称是分液漏斗,滴加液体的操作是打开先将上口的玻璃塞打开,然后选择活塞使分液漏斗中的液体缓缓流下
(3)两个洗气瓶中所装的液体分别是饱和食盐水;浓硫酸.
(4)某同学在实验中,发现量筒中未收集到液体,则失败的原因可能是没有氯气产生或产生的氯气被溶液吸收或是装置漏气.
(5)结合方程式加以解释,为什么氯气不可漂白干燥的有色布条?氯气不具有漂白性,有漂白性的次氯酸,而干燥布条不含水,不能发生反应:Cl2+H2O=HCl+HClO,生成次氯酸,所以布条不褪色.
分析 (1)依据实验目的及各装置作用:制备氯气,除去氯化氢,干燥氯气,验证氯气的漂白性,排水法测气体的体积;
(2)依据图中仪器形状说出其名称,依据分液漏斗使用方法解答;
(3)浓盐酸易挥发,制取的氯气中含有氯化氢和水蒸气,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,浓硫酸具有吸水性,能够干燥氯气;
(4)量筒中未收集到液体,说明没有氯气生成或氯气被其它物质吸收或漏气;
(5)氯气不具有漂白性,具有漂白性的是次氯酸.
解答 解:(1)本实验有两个目的,其一是验证干燥的氯气没有漂白性;其二是测量氯气的体积.由于测量氯气的体积是根据排入量筒里的水来读出,所以验证干燥的氯气无漂白性的实验必须放在测量氯气的体积之前(否则无法连接),所以其连接顺序:发生装置→除氯化氢杂质→除水蒸气→验证漂白性→排液体→收集液体,除去水蒸气可以用装有无水CaCl2的U型管,也可以用盛有浓硫酸的洗气瓶,则连接顺序是:a接d、e接b或c、c或b接g、h接e、d接f,
故答案为:d;e;b或c;c或b;g;h;e;d;f;
(2)图中滴加液体的仪器为分液漏斗,使用分液漏斗正确方法:先将上口的玻璃塞打开,然后选择活塞使分液漏斗中的液体缓缓流下;
故答案为:分液漏斗;先将上口的玻璃塞打开,然后选择活塞使分液漏斗中的液体缓缓流下;
(3)浓盐酸易挥发,制取的氯气中含有氯化氢和水蒸气,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以选择饱和食盐水除去氯化氢;浓硫酸具有吸水性,能够干燥氯气;
故答案为:饱和食盐水;浓硫酸;
(4)量筒中未收集到液体,可能是没有氯气产生或产生的氯气被溶液吸收或是装置漏气,故答案为:没有氯气产生或产生的氯气被溶液吸收或是装置漏气;
(5)氯气不具有漂白性,氯气与水反应生成次氯酸,方程式:Cl2+H2O=HCl+HClO,次氯酸具有漂白性,干燥布条没有水,不能生成次氯酸,所以不褪色,
故答案为:氯气不具有漂白性,有漂白性的次氯酸,而干燥布条不含水,不能发生反应:Cl2+H2O=HCl+HClO,生成次氯酸,所以布条不褪色.
点评 本题考查探究氯气的性质,难点是将装置进行排序,根据实验目的来分析解答即可,难度较大.

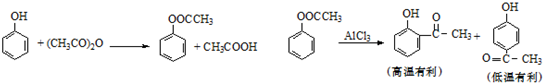
(1)乙酸苯酚酯制备:
将9.4g苯酚溶解在60mL10%的氢氧化钠溶液中,加入30g碎冰块,然后加入13.0g乙酸酐,搅拌5min.将反应后混合物倾入分液漏斗中,加入约4mL CCl4.将有机相用试剂X和水洗涤然后无水CaCl2干燥,蒸馏收集193-197℃馏分.
①用碎冰块代替水可能的原因是:该反应是放热反应,碎冰温度低有利于酯的生成.
②乙酸酐过量的目的是:提高苯酚的转化率.
③有机相先用试剂X洗涤,X可能是Na2CO3或NaHCO3溶液.
(2)对羟基苯乙酮的制备:
将乙酰苯酚6.8g,硝基苯20mL 放在三口烧瓶中,搅拌下加入无水AlCl3 11g(此时放热),加完后控制合适的温度,维持一定时间.然后冷却,倾入冰水中,用6mol/L HCl酸化分出硝基苯层,水层用氯仿萃取,蒸出氯仿得粗品.
①硝基苯的作用是作溶剂.
②乙酸苯酚重排为对羟基苯乙酮反应条件对收率的影响关系如表
| 反应温度/℃ | 反应时间(min) | 收率 |
| 30~35 | 180 | 10.0 |
| 20~25 | 60 | 18.0 |
| 20~25 | 120 | 26.0 |
| 20~25 | 180 | 58.5 |
| A. | 淀粉和纤维素的通式都是(C6H10O5)n,是同分异构体 | |
| B. | 向鸡蛋清溶液中加入(NH4)2SO4饱和溶液,有沉淀析出,再加水沉淀不溶解 | |
| C. | 油脂、糖类和蛋白质是食物含有的主要营养物质,它们都是高分子化合物 | |
| D. | 可以用新制的Cu(OH)2悬浊液检验患者的尿液中是否含糖 |
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:BKNO3,DCuSO4.
(2)在A溶液中加入少量澄清石灰水,观察到的现象为产生白色沉淀
(3)将含lmol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为Na2CO3.反应的离子方程式是HCO3-+OH-=H2O+CO32-.
(4)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3(胶体)+3H+.
| A. | 推广使用燃煤脱硫技术,在燃煤中加入适量石灰石,可减少废气中的SO2 | |
| B. | 实施绿化工程,防治扬尘污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加高工厂的烟囱,使烟尘和废气远离地表 |
| A. | 溶液呈电中性,胶体带有电荷 | |
| B. | 溶液中溶质微粒一定带电,胶体中分散质粒子带电,且通电后,溶质粒子向两极移动,胶体粒子向一极移动 | |
| C. | 溶液中溶质粒子有规律运动,而胶体粒子无规律运动 | |
| D. | 溶液中通过一束光线时无特殊现象,胶体中通过一束光时有明显的光带 |
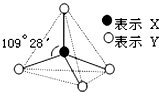 甲、乙、丙、丁、戊具有如图所示的结构或结构单元,图中四面体外可能有的部分未画出,只有实线表示共价键,X、Y可同可不同.
甲、乙、丙、丁、戊具有如图所示的结构或结构单元,图中四面体外可能有的部分未画出,只有实线表示共价键,X、Y可同可不同.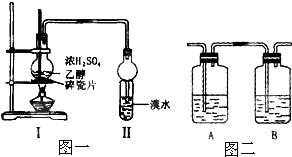 某化学兴趣小组用图一所示装置进行探究实验.以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.
某化学兴趣小组用图一所示装置进行探究实验.以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.