题目内容
6. A、B、C、D、E是含有一种相同元素的五种物质,一定条件下可发生如图所示的转化.其中A是单质,B是常见的10电子体分子,E是含氧酸,回答问题.
A、B、C、D、E是含有一种相同元素的五种物质,一定条件下可发生如图所示的转化.其中A是单质,B是常见的10电子体分子,E是含氧酸,回答问题.(1)化学方程式:①(B→C)4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O②(D+B,一定条件)8NH3+6NO2$\frac{\underline{\;一定条件\;}}{\;}$7N2+12H2O离子方程式:③(E→C)3Cu+8H++2NO3-(稀)═3Cu2++2NO?+4H2O④(E稀+SO2气体)3SO2+2H2O+2NO3-=2NO↑+4H++3SO42-.
(2)以N2、H2、O2及H2O为主要原料制取硝酸铵最少4步化学反应就能完成,并且理论上无尾气放出.
(3)在反应②中,氧化产物与还原产物之比为4:3.
分析 A、B、C、D、E是含有一种相同元素的五种物质,A是单质,E是含氧酸,B是常见的10电子气体分子,B是NH3,则A是N2,C是NO,D是NO2,E是HNO3,符合题中各物质的转化关系,以此解答该题.
解答 解:A、B、C、D、E是含有一种相同元素的五种物质,A是单质,E是含氧酸,B是常见的10电子气体分子,B是NH3,则A是N2,C是NO,D是NO2,E是HNO3,符合题中各物质的转化关系,
(1)①B→C的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,②D+B的化学方程式为8NH3+6NO2$\frac{\underline{\;一定条件\;}}{\;}$7N2+12H2O,③E→C的离子方程式为3Cu+8H++2NO3-(稀)═3Cu2++2NO?+4H2O,④E稀+SO2气体的离子方程式为3SO2+2H2O+2NO3-=2NO↑+4H++3SO42-,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;8NH3+6NO2$\frac{\underline{\;一定条件\;}}{\;}$7N2+12H2O;3Cu+8H++2NO3-(稀)═3Cu2++2NO?+4H2O;3SO2+2H2O+2NO3-=2NO↑+4H++3SO42-;
(2)以N2、H2、O2及H2O为主要原料制取硝酸铵最少的步骤为用氮气与氢气反应生成氨气,氨气与氧气反应生成一氧化氮,一氧化氮与氧气、水生成硝酸,硝酸与氨气反应生成硝酸氨,共4步化学反应就能完成,并且理论上无尾气放出,
故答案为:4;
(3)根据反应②的方程式可知,发生还原反应的二氧化氮中氮元素得到还原产物,发生氧化反应的是氨气中的氮元素得到氧化产物,这两种物质的物质的量之比为3:4,所以氧化产物与还原产物之比为4:3,
故答案为:4:3.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,题目难度不大,本题注意根据物质的结构如10电子分子等及各物质的相互转化的关系特征为突破口进行推断.

 阅读快车系列答案
阅读快车系列答案| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
| A. | 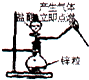 | B. |  | C. |  | D. |  |
| A. | 摩尔既是物质的数量单位又是物质的质量单位 | |
| B. | 物质的量是国际单位制中七个基本单位之一 | |
| C. | 阿伏加德罗常数是0.012kg 12C中含有的碳原子数目 | |
| D. | 标准状况下,1molH2O所占的体积为22.4L |
| A. | 用量筒量取一定量液体时,先从试剂瓶中直接倒入大部分试剂于量筒中,至接近刻度时改用胶头滴管,逐滴加入至刻度 | |
| B. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| C. | N2O5在四氯化碳溶液中分解为NO2和O2,可用分光光度计测定其化学反应速率 | |
| D. | 物质的分离提纯方法之一为“筛分:如胶体--半透膜法分离提纯;悬浊液--过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的筛子 |
| A. | 在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O22CO2+2CaSO4 | |
| B. | CO2通入水玻璃可以得到硅酸沉淀 Na2SiO3+CO2+H2O═Na2CO3+H2SiO3↓ | |
| C. | 硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 | |
| D. | 氢氟酸能够雕刻玻璃,故不能用玻璃瓶在盛装氢氟酸 SiO2+4HF═SiF4↑+2H2O |
| A. | 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 25℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小 | |
| D. | 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
 )4种有机物分别在一定条件下与H2充分反应.
)4种有机物分别在一定条件下与H2充分反应.