题目内容
8.下列叙述正确的是( )| A. | 甲醇(CH3OH)和乙醇互为同系物 | |
| B. | 不同元素的原子构成的分子只能含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同质子数相同的同种核素 | |
| D. | 短周期第IVA与VIIA族元素的原子间构成的分子,均不满足原子最外层8电子结构 |
分析 A.结构相似,分子组成上相差1个或多个CH2原子团的有机物互为同系物;
B.H、O形成的化合物中能存在非极性共价键;
C.质子数相同,中子数不同的同种元素的不同核素互为同位素;
D.原子最外层电子数与其化合价绝对值之和为8,满足8电子结构.
解答 解:A.甲醇(CH3OH)和乙醇结构相似,分子组成上相差1个原子团CH2,属于同系物,故A正确;
B.H、O形成的化合物中能存在非极性共价键,如过氧化氢中存在极性键和非极性共价键,故B错误;
C.二者质子数相同,但是中子数不同,属于不同核素,互为同位素,故C错误;
D.短周期第IVA族与VIIA族元素的原子间构成的分子为AB4型,原子最外层电子数与其化合价绝对值之和均为8,满足8电子结构,故D错误;
故选A.
点评 本题考查了同素异形体的概念,极性键和非极性共价键的判断等,题目难度不大,注意相关知识的积累.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
13.钾是活泼的碱金属,钾和氧气反应时可以生成氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物,现将钾与氧气在一定条件下的反应产物溶于水,所得溶液用HCl溶液进行反应,终点时消耗HCl为73g,则单质钾的质量为( )
| A. | 39g | B. | 59g | C. | 78g | D. | 97g |
16.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为9NA | |
| B. | 1 L 0.2 mol•L-1硫酸铁溶液中含有的SO42-数为0.2NA | |
| C. | 0.1mol N2与足量的H2反应,转移的电子数为0.6NA | |
| D. | 用惰性电极电解1L0.1mol•L-1 CuCl2溶液,当有0.2NA个电子通过时,可生成6.4g铜 |
3.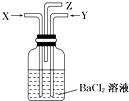 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | B. | 在Z导管出来的气体中无二氧化碳 | ||
| C. | 洗气瓶中产生的沉淀是硫酸钡 | D. | 在Z导管口有红棕色气体出现 |
13.下列说法正确的是( )
| A. | 化学反应进行的越快,化学反应现象越明显 | |
| B. | 某反应中,经2min后B浓度减少0.6mol•L-1,在2min时用B表示的反应速率为0.6mol•L-1•min | |
| C. | 化学反应中的能量变化都是化学能转化成热能 | |
| D. | 原电池的反应一定是氧化还原反应 |
20.在同温同压下,某有机物和过量的金属钠反应得到V1L氢气,另一份等量的该有机物和足量的NaHCO3反应得V2 L二氧化碳(均为标况),若Vl=V2≠O,则此有机物可能是( )
| A. | HO-CH2CH2-COOH | B. | HOOC-COOH | C. | HO-CH2CH2-OH | D. | CH2-COOH |
17.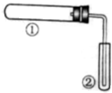 用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
 用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 | |
| Ⅰ | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| Ⅱ | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| Ⅲ | NaHCO3 | 澄清石灰水变浑浊 |
| A. | 只有Ⅰ | B. | 只有Ⅱ | ||
| C. | 只有Ⅲ | D. | Ⅰ、Ⅱ、Ⅲ均能证实①中反应发生 |
 .
.