��Ŀ����
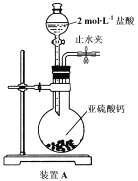
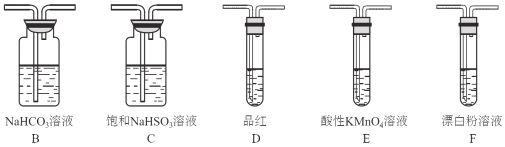
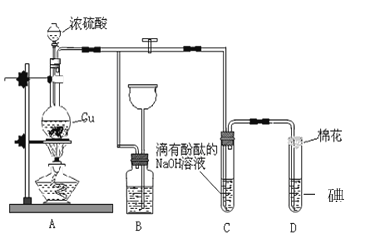
����Ŀ����������Ҫ�ɷ���MoS2(Mo��+4��)��������SiO2�Լ�Re�Ļ���������ʡ��ɻ������Ƶý�����ʴ�������ƾ���(Na2MoO4��10H2O)������Mo2C��������KReO4������Ҫ�������£�

(1)���ջ����ʱ�����ķ�Ӧ����Ӧ��ʼ���¶�(T)����նȵĹ�ϵ����ͼ��ʾ��(��ն�P/P0��ʾ��Ӧʱ��ѹǿ�������ѹ֮��)
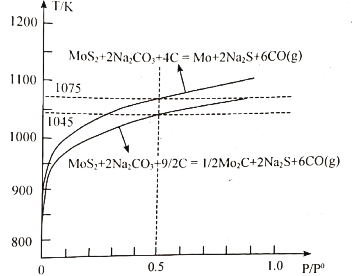
Ϊ���̼���⣬����ն�Ϊ0.5�������£����˵ķ�Ӧ�¶�Ӧ����___________��
(2)����ʱ������Mo2C�ķ�Ӧ�б���ԭ��Ԫ����___________(��Ԫ�ط���)��ˮϴ�ս���ʱ��ϴȥ�����ʳ�Na2S��Na2CO3֮�⣬����___________��
(3)�� NaClO2����MoS2ʱ��MoS2ת��ΪMoO42-��SO42-��д���÷�Ӧ�����ӷ���ʽ___________��
(4)��֪�����Ƶ��ܽ����������ͼ�����Na2MoO4��10H2O�IJ���AΪ___________��___________�����ˡ�

(5)����KReO4����Ļ�ѧ����ʽΪ___________������KClʱ��ͬʱ�����Ҵ���������___________��
���𰸡�1045K��T<1075K Mo��C Na2SiO3 2MoS2+9ClO2-+12OH- =2MoO42-+9Cl-+4SO42-+6H2O ����Ũ�� ��ȴ��10�����½ᾧ NaReO4+KCl=KReO4��+NaCl ��СKReO4���ܽ��
��������
(1)���ݷ�Ӧ��ʼʱ��������Ӧ���¶ȷ�����Ӧ������
(2)����Ԫ�ػ��ϼ����ߣ�ʧȥ���ӱ�������Ԫ�ػ��ϼ۽��ͣ���õ��ӣ�����ԭ�����жϣ�
������ʱ����������Ӧ2MoS2+4Na2CO3+9C![]() Mo2C+4Na2S+12C(g)�⣬��������Ӧ��SiO2+Na2CO3
Mo2C+4Na2S+12C(g)�⣬��������Ӧ��SiO2+Na2CO3![]() Na2SiO3+CO2�����������ʵ��ܽ��Է���ϴȥ�����ʣ�
Na2SiO3+CO2�����������ʵ��ܽ��Է���ϴȥ�����ʣ�
(3)NaClO2���������ԣ�������MoS2ΪMoO42-��SO42-��NaClO2����ԭΪCl-�����ݵ����غ㡢����غ㼰ԭ���غ���ƽ��Ӧ����ʽ��
(4)���� Na2MoO4��10H2O���ܽ���ڵ���10��ʱ�¶����ߣ��ܽ�����������
(5)��NaReO4����Һ�м���KCl���Ҵ�����Ӧ�õ�KReO4��˵�������˸��ֽⷴӦ��KReO4���Ҵ����ܽ��С��
(1) ���¶�Ϊ1045K ʱ��Ӧ2MoS2+4Na2CO3+9C![]() Mo2C+4Na2S+12C(g)�ſ�ʼ�����������¶ȸ���1075K�ᷢ������ӦMoS2+2Na2CO3+4C
Mo2C+4Na2S+12C(g)�ſ�ʼ�����������¶ȸ���1075K�ᷢ������ӦMoS2+2Na2CO3+4C![]() Mo+2Na2S+6CO(g)������Mo��ʵ�鷴Ӧ�¶�Ҫ������1045K��T<1075K��
Mo+2Na2S+6CO(g)������Mo��ʵ�鷴Ӧ�¶�Ҫ������1045K��T<1075K��
(2)����ʱ����2MoS2+4Na2CO3+9C![]() Mo2C+4Na2S+12C(g)����Ӧ��MoԪ�صĻ��ϼ��ɷ�Ӧǰ��+4�۱�Ϊ��Ӧ���+2�ۣ�CԪ�صĻ��ϼ��ɷ�Ӧǰ��+4�۱�Ϊ��Ӧ��Mo2C�е�-4�ۡ�����C��0�ۣ����ϼ۽��ͣ����Ա���ԭ��Ԫ������Mo��C��������ʱ��������2MoS2+4Na2CO3+9C
Mo2C+4Na2S+12C(g)����Ӧ��MoԪ�صĻ��ϼ��ɷ�Ӧǰ��+4�۱�Ϊ��Ӧ���+2�ۣ�CԪ�صĻ��ϼ��ɷ�Ӧǰ��+4�۱�Ϊ��Ӧ��Mo2C�е�-4�ۡ�����C��0�ۣ����ϼ۽��ͣ����Ա���ԭ��Ԫ������Mo��C��������ʱ��������2MoS2+4Na2CO3+9C![]() Mo2C+4Na2S+12C(g)��Ӧ�⣬ԭ���е�����SiO2��Na2CO3��Ӧ��SiO2+Na2CO3
Mo2C+4Na2S+12C(g)��Ӧ�⣬ԭ���е�����SiO2��Na2CO3��Ӧ��SiO2+Na2CO3![]() Na2SiO3+CO2��������ˮϴ�ս��ϴȥ�����ʳ�Na2S��Na2CO3֮�⣬���п����Ե�Na2SiO3��
Na2SiO3+CO2��������ˮϴ�ս��ϴȥ�����ʳ�Na2S��Na2CO3֮�⣬���п����Ե�Na2SiO3��
Ҫ���Na2MoO4��10H2O��������10�����½ᾧ�����������Na2MoO4��2H2O ���塣����KReO4�ܽ��С��NaReO4����ʵ����NaReO4��KReO4��ת���������Ҵ��ɽ���KReO4���ܽ�ȣ�������KReO4����������
(3)�� NaClO2����MoS2ʱ��MoS2ת��ΪMoO42-��SO42-��NaClO2����ԭΪCl-�����ݵ����غ㡢����غ㼰ԭ���غ㣬�ɵ÷�Ӧ�����ӷ���ʽ��2MoS2+9ClO2-+12OH- =2MoO42-+9Cl-+4SO42-+6H2O��
(4)�����ܽ�����߿�֪�� Na2MoO4��10H2O���ܽ���ڵ���10��ʱ�¶����ߣ��ܽ�������¶ȸ���10��ʱ��ת��ΪNa2MoO4��2H2O����Ҫ���Na2MoO4��10H2O��Ӧ�ý��еIJ���������Ũ���õ�10��ʱ�ı�����Һ��Ȼ����ȴ��10�����½ᾧ�����ˣ��Ϳɵõ�Na2MoO4��10H
(5)���������֪NaReO4��KCl�������ֽⷴӦ�������ܽ��С��KReO4����Ӧ�Ļ�ѧ����ʽ��NaReO4+KCl=KReO4��+NaCl������KClʱ��ͬʱ�����Ҵ��������ǽ���KReO4���ܽ�ȡ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ�������������������������������Ҫ�����á��ش��������⣺
(1)��֪4NH3(g)+5O2(g)=4NO(g)+6H2O(g)��H1=��alkJ/mol��4NH3(g)+6NO(g)=5N2(g)+6H2O(g)��H2=��bkJ/mol��H2O(1)=H2O(g)��H3=+ckJ/mol��д����298Kʱ������ȼ������N2���Ȼ�ѧ����ʽ___________��
(2)�����еļ��쵰��(Mb)����O2�������MbO2��Mb(aq)+O2(g)![]() MbO2(aq)������k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ�������V��=k����c(Mb)��P(O2)��V��=k����c(MbO2)��37��ʱ��ü��쵰�Ľ�϶�(��)��P(O2)�Ĺ�ϵ���±�[��϶�(��)ָ����O2��ϵļ��쵰��ռ�ܼ��쵰�İٷֱ�]��
MbO2(aq)������k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ�������V��=k����c(Mb)��P(O2)��V��=k����c(MbO2)��37��ʱ��ü��쵰�Ľ�϶�(��)��P(O2)�Ĺ�ϵ���±�[��϶�(��)ָ����O2��ϵļ��쵰��ռ�ܼ��쵰�İٷֱ�]��
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
����MbO2%�� | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
�ټ���37�桢P(O2)Ϊ2.00kPaʱ��������Ӧ��ƽ�ⳣ��K=___________��
�ڵ���ƽ��ʱ���쵰����O2�Ľ�϶�(��)��O2��ѹǿ[P(O2)]֮��Ĺ�ϵʽ��=___________(�ú���k����k����ʽ�ӱ�ʾ)��
(3)���ɼ��쵰�ĸʰ���(NH2CH2COOH)��һ���������ʣ�����Һ��������������ʽ���ڣ���ת����ϵ���£�
![]()
![]()
![]()
![]()
![]()
�ڸʰ�����Һ�м�������������ӵİٷֺ�����![]() �Ĺ�ϵ��ͼ��ʾ��
�Ĺ�ϵ��ͼ��ʾ��

�ٴ��ʰ�����Һ��___________�ԣ�����Һ������ʱ�������ӵ�Ũ���ɴ�С��˳��Ϊ___________��
����![]() =8����Һ�м������HClʱ����Ӧ�����ӷ���ʽΪ___________��
=8����Һ�м������HClʱ����Ӧ�����ӷ���ʽΪ___________��
���õ�λ�ζ����ɲⶨij�ʰ�����Ʒ�Ĵ���.
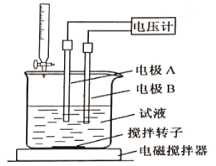
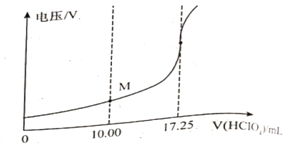
��ȡ��Ʒ150mg����һ�������£���0.1000mol/L�ĸ�������Һ�ζ�(��ʰ���1�U1������Ӧ)����õ�ѹ�仯�����HClO4��Һ�������ϵ����ͼ�����հ���ʵ�飬����HClO4��Һ�����Ϊ0.25mL������Ʒ�Ĵ���Ϊ___________%(����������һλС��)