题目内容
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用。可通过以下方法合成:


⑴化合物A中所含官能团的名称为______和______。
⑵由F→G的反应类型是______。
⑶D的结构简式为______。
⑷写出同时满足下列条件的C的一种同分异构体的结构简式:______。
①能发生银镜反应,与FeCl3溶液不显色;
②能发生水解反应,水解产物之一能与FeCl3溶液显色;
③分子中含有4种不同化学环境的氢。
⑸请写出以苯甲酸、甲醇为原料制备![]() 的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
【答案】羧基 羟基 消去反应 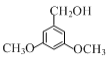
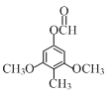 或
或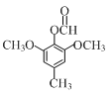
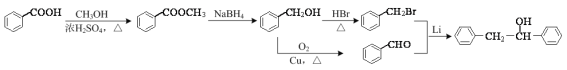
【解析】
B发生酯化反应得到C,则C的结构简式为:![]() ,C与硼氢化钠发生还原反应生成D,D与HBr发生取代反应生成E,根据D的分子式和E的结构简式可知D的结构简式为
,C与硼氢化钠发生还原反应生成D,D与HBr发生取代反应生成E,根据D的分子式和E的结构简式可知D的结构简式为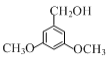 ,E发生加成反应生成F,结合G的分子式推知F在浓硫酸作用下发生了消去反应,生成G的结构简式为:
,E发生加成反应生成F,结合G的分子式推知F在浓硫酸作用下发生了消去反应,生成G的结构简式为:![]() ,G和三溴化硼反应生成白藜芦醇,据此分析作答。
,G和三溴化硼反应生成白藜芦醇,据此分析作答。
⑴化合物A为中所含官能团为羧基和羟基,故答案为:羧基;羟基;
⑵F在浓硫酸作用下发生了消去反应生成G,故答案为:消去反应;
⑶根据上述分析可知,D的结构简式为 ;
;
⑷C为![]() ,分子式为:C10H12O4,不饱和度为
,分子式为:C10H12O4,不饱和度为![]() =5,,①能发生银镜反应,与FeCl3溶液不显色,说明分子内含醛基,不含酚羟基;②能发生水解反应,水解产物之一能与FeCl3溶液显色,说明含有酯基;③分子中含有4种不同化学环境的氢,则符合上述条件的同分异构体为:
=5,,①能发生银镜反应,与FeCl3溶液不显色,说明分子内含醛基,不含酚羟基;②能发生水解反应,水解产物之一能与FeCl3溶液显色,说明含有酯基;③分子中含有4种不同化学环境的氢,则符合上述条件的同分异构体为: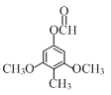 或
或 ;
;
⑸根据给出的合成路线,可知,苯甲酸可先与甲醇发生酯化反应生成苯甲酸甲酯,然后在硼氢化钠作用下发生换换反应生成苯甲醇,再与HBr发生取代反应生成![]() ,同时苯甲醇与氧气发生催化氧化生成苯甲醛,最后根据E到F的合成思路纸杯所需目标产物,具体合成路线 如下:
,同时苯甲醇与氧气发生催化氧化生成苯甲醛,最后根据E到F的合成思路纸杯所需目标产物,具体合成路线 如下: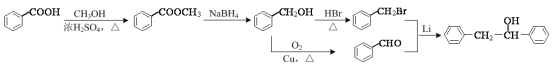 。
。

【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)写出元素符号和名称:
①________,②________,⑧________,⑨________。
(2)写出下列反应的化学方程式:
⑤的氧化物跟④的氢氧化物溶液反应:________________________________
⑥的单质在③的单质中燃烧:_____________________________________。
【题目】高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s) + CO(g)
Fe2O3(s) + CO(g) ![]()
![]() Fe(s) + CO2(g)。已知该反应在不同温度下的平衡常数如下:
Fe(s) + CO2(g)。已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(CO2)=______________________、CO的平衡转化率= _____________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
(4)在1L的密闭容器中,1300℃条件,下列达平衡状态的是_______________。
A | B | C | D | |
n(Fe2O3) | 0.350 | 0.027 | 0.080 | 0.080 |
n(CO) | 0.010 | 0.010 | 0.010 | 0.050 |
n(Fe) | 0.100 | 0.064 | 0.080 | 0.080 |
n(CO2) | 0.035 | 0.088 | 0.040 | 0.050 |
.