题目内容
19.已知含氧酸可用通式(OH)nXOm来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4.一般而言,该式中m大的是强酸,m小的是弱酸,下列各含氧酸中酸性最强的是( )| A. | H2SeO3 | B. | HMnO4 | C. | H3BO3 | D. | H3PO4 |
分析 含氧酸可用通式(OH)nXOm表示,该式中m大的是强酸,m小的是弱酸,将各含氧酸用通式表示,根据m个数多少判断酸性强弱,据此分析解答.
解答 解:含氧酸可用通式(OH)nXOm表示,该式中m大的是强酸,m小的是弱酸,
A.H2SeO3用通式表示为(OH)2SeO,m=1;
B.HMnO4用通式表示为(OH)MnO3,m=3;
C.H3BO3用通式(OH)3BO0表示,m=0;
D.H3PO4用通式(OH)3PO1表示,m=1;
通过以上分析知,B中m最大,则B的酸性最强,故选B.
点评 本题考查物质结构和性质的关系,侧重考查知识迁移能力,正确理解并灵活运用题给信息是解本题关键,由此得出正确判断,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
10.有原子序数依次增大的A、B、C、D、E五种短周期元主族素,它们可两两组成甲、乙、丙、丁四种化合物,各化合物中原子个数比关系如下表:
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多两个;在周期表中,C是E的邻族元素,化学性质活泼;D和E位于同一周期,且D和E的原子序数之和为30.
(1)甲的电子式 ,丁的结构式
,丁的结构式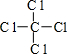
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.
(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)甲的电子式
 ,丁的结构式
,丁的结构式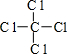
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为
 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
14.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 沸点:乙烷>戊烷>2-甲基丁烷 | B. | 熔点:Al>Na>Na和K的合金 | ||
| C. | 密度:苯<水<1,1,2,2-四溴乙烷 | D. | 热稳定性:HF>HCl>H2S |
11.属于苯的同系物是( )
| A. | 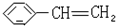 | B. | 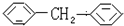 | C. |  | D. | 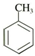 |
8.能说明某烃分子里含有碳碳不饱和键的是( )
| A. | 分子组成中含碳氢原子个数比为1:2 | |
| B. | 能与溴发生加成反应而使溴水褪色,还能使酸性KMnO4溶液褪色 | |
| C. | 在空气中燃烧能产生黑烟 | |
| D. | 完全燃烧生成等物质的量的CO2和H2O |
9.下列变化需克服相同类型作用力的是( )
| A. | 碘和干冰的升华 | B. | 硅和冰的熔化 | ||
| C. | 氯化氢和氯化钾的溶解 | D. | 氯化钠和冰融化 |
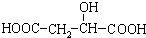 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山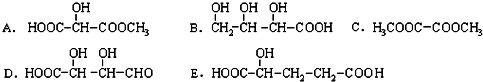

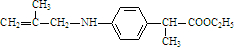 .
.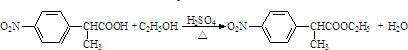 .
.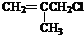 有相同官能团的同分异构体有10种.(要求考虑顺反异构)
有相同官能团的同分异构体有10种.(要求考虑顺反异构)