题目内容
5.关于化学反应与能量的说法中不正确的是( )| A. | 中和反应是放热反应 | |
| B. | 右图所示的反应为放热反应 | |
| C. | 化学反应中有物质变化也有能量变化 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
分析 化学反应的实质为化学键的断裂和形成,断裂化学键吸收能量,形成化学键放出能量,则化学反应有物质变化也有能量变化,从宏观角度分析,生成物总能量大于反应物总能量,则正反应为吸热反应,反之为放热反应,常见放热反应有中和、化合以及物质的燃耗,活泼金属与酸的反应等,以此解答该题.
解答 解:A.中和反应是放热反应,如氢氧化钠与硫酸的反应,故A正确;
B.生成物总能量大于反应物总能量,则正反应为吸热反应,故B错误;
C.化学反应的实质为化学键的断裂和形成,断裂化学键吸收能量,形成化学键放出能量,则化学反应有物质变化也有能量变化,故C正确;
D.化学键断裂,形成自由原子,能量较高,则为吸收能量,生成化学键,物质能量降低,则放出能量,故D正确.
故选B.
点评 本题考查学生化学反应中的能量变化知识,为高频考点,侧重于基本概念的综合理解和运用的考查,注意据反应物的总能量和生成物的总能量之间的关系来确定反应的吸放热的结论,难度不大.

练习册系列答案
相关题目
18.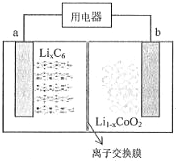 某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
 某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )| A. | 放电时,电子从b极流向a极 | |
| B. | 放电时,a极脱出的离子通过阴离子交换膜从左向右移动 | |
| C. | 充电时,b极发生的反应为:LiCoO2-xe-=Li1-xCoO2+xLi+ | |
| D. | 充电时,每转移x mol 电子,产生6mol碳单质 |
17.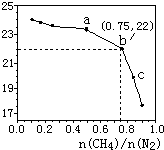 已知:在700℃的恒温、恒容密闭容器中发生反应3CH4(g)+2N2(g)?3C(s)+4NH3(g),若CH4与N2在不同投料比$\frac{n(C{H}_{4})}{n({N}_{2})}$时CH4的平衡转化率如图所示,下列说法正确的是( )
已知:在700℃的恒温、恒容密闭容器中发生反应3CH4(g)+2N2(g)?3C(s)+4NH3(g),若CH4与N2在不同投料比$\frac{n(C{H}_{4})}{n({N}_{2})}$时CH4的平衡转化率如图所示,下列说法正确的是( )
 已知:在700℃的恒温、恒容密闭容器中发生反应3CH4(g)+2N2(g)?3C(s)+4NH3(g),若CH4与N2在不同投料比$\frac{n(C{H}_{4})}{n({N}_{2})}$时CH4的平衡转化率如图所示,下列说法正确的是( )
已知:在700℃的恒温、恒容密闭容器中发生反应3CH4(g)+2N2(g)?3C(s)+4NH3(g),若CH4与N2在不同投料比$\frac{n(C{H}_{4})}{n({N}_{2})}$时CH4的平衡转化率如图所示,下列说法正确的是( )| A. | n(CH4)/n(N2)越大,CH4的转化率越高 | |
| B. | a点对应的平衡常数比c点的大 | |
| C. | b点对应的NH3的体积分数为26% | |
| D. | 不改变投料比,增加n(N2)时,NH3体积分数增大 |
13.对羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得.下列有关说法正确的是( )


| A. | 对羟基扁桃酸可以发生消去反应、取代反应和缩聚反应 | |
| B. | 苯酚和对羟基扁桃酸是同系物 | |
| C. | 乙醛酸与H2在热的镍催化下反应生成乙二醇 | |
| D. | 在核磁共振氢谱中对羟基扁桃酸应该有6个吸收峰 |
20. 利用人工模拟光合作用合成甲酸的原理为:
利用人工模拟光合作用合成甲酸的原理为:
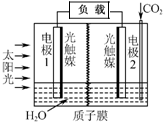
太阳能光触媒2CO2+2H2O $→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
 利用人工模拟光合作用合成甲酸的原理为:
利用人工模拟光合作用合成甲酸的原理为:太阳能光触媒2CO2+2H2O $→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
| A. | 电极1周围pH增大 | |
| B. | 电子由电极1经过负载流向电极2 | |
| C. | 电极2的反应式:CO2+2H++2e-=HCOOH | |
| D. | 该装置能将太阳能转化为化学能和电能 |
10.下列装置能达到对应实验目的是( )
| A. |  分离碘与沙子 | B. | 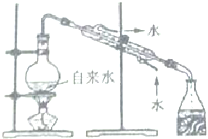 实验室制取蒸馏水 | ||
| C. | 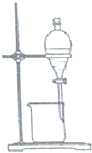 乙醇提取碘水中的碘 | D. | 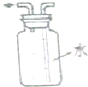 收集氨气 |
17. X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
 X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )| A. | 简单离子的半径:X3+>Z3- | |
| B. | 元素Z的最外层电子可能为6 | |
| C. | 元素Y的最高价氧化物的水化物可能是强酸 | |
| D. | 元素W的最高价氧化物的水化物属于共价化合物 |
14.只用一种试剂就能将甲苯、己烯、四氯化碳和碘化钾溶液区分开,该试剂可以是( )
| A. | 酸性高锰酸钾溶液 | B. | 溴化钠溶液 | ||
| C. | 溴水 | D. | 硝酸银溶液 |
12. 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )| A. | 该烃X与等质量的甲烷相比,X燃烧时消耗的氧气更多 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 分子中的氢原子分布在两个互相垂直的直线上 | |
| D. | 分子中有C-C键,也有C=C键 |