题目内容
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.1 mol OD﹣离子含有的质子、中子数均为10NA
B.标准状况下,4.48 L己烷含有的分子数为0.2NA
C.标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.2NA
D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
【答案】D
【解析】解:A.1个OD﹣离子含有的质子、中子数均为9,则1 mol OD﹣离子含有的质子、中子数均为9NA , 故A错误; B.标况下,己烷是液体,气体摩尔体积对其不适用,所以无法计算己烷的物质的量,导致无法计算己烷分子个数,故B错误;
C.标况下n(NO2)= ![]() =0.3mol,二氧化氮和水反应方程式为3NO2+H2O=2HNO3+NO,该反应中作氧化剂和还原剂的二氧化氮物质的量之比为1:2,所以参加反应的二氧化氮有0.1mol作氧化剂,即标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.1NA , 故C错误;
=0.3mol,二氧化氮和水反应方程式为3NO2+H2O=2HNO3+NO,该反应中作氧化剂和还原剂的二氧化氮物质的量之比为1:2,所以参加反应的二氧化氮有0.1mol作氧化剂,即标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.1NA , 故C错误;
D.丙烯和环丙烷互为同分异构体,n(C3H6)= ![]() =1mol,每个分子中含有6个H原子,则氢原子的物质的量是6mol,即氢原子的个数为6NA , 故D正确;
=1mol,每个分子中含有6个H原子,则氢原子的物质的量是6mol,即氢原子的个数为6NA , 故D正确;
故选D.

【题目】利用右图所示装置进行下列实验,能得到相应实验结论的是 ( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | Na2SO3 | KMnO4溶液褪色 | SO2有漂白性 | |
B | 浓盐酸 | KMnO4 | FeBr2溶液变为黄色 | 氧化性:Cl2 >Br2 | |
C | 稀硫酸 | 碳酸钠 | CaCl2溶液无明显变化 | CO2不与CaCl2反应 | |
D | 浓硫酸 | 蔗糖 | 溴水褪色 | 浓硫酸具有脱水性、吸水性 |
A.A
B.B
C.C
D.D
【题目】下列实验操作说法正确的是( )
选项 | 实验操作 | 现象与结论(或装置用途) |
A | 某溶液加入浓NaOH溶液加热,在试管口放一片湿润的红色石蕊试纸 | 试纸变蓝,说明NH3是碱 |
B |
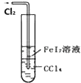
| 可以用于比较Fe3+、I2、Cl2的氧化性强弱 |
C | 2mL 2% CuSO4中加4~6滴2% NaOH溶液,振荡后加入0.5mL X溶液,加热煮沸 | 未出现砖红色沉淀,说明X不含有醛基 |
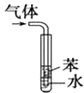
D |
| 用于吸收HCl气体能防倒吸 |
A.A
B.B
C.C
D.D