题目内容
已知25%的氨水的密度为0.91 g/ml,5%的氨水密度为0.98 g/ml,若将上述两种氨水等体积混合,所得氨水的质量分数 ( )
| A.等于15% | B.大于15% | C.小于15% | D.无法确定 |
C
解析试题分析:由于氨水的浓度越大,溶液的密度越小,则两种氨水等体积混合后,25%的氨水溶液的质量小于5%的氨水溶液中的质量,所以二者混合后,所得氨水的质量分数小于两溶液溶质质量分数的平均值,即小于15%,答案选C。
考点:考查氨水溶液混合后溶液质量分数的有关计算
点评:该题是中等难度的试题,试题难易适中,注重答题的灵活性。该类试题需要注意的是当浓度越大其密度越小的同溶质不同浓度的水溶液等体积相混,所得混合后的溶液溶质的质量分数小于混合前的两溶液溶质质量分数的平均值,反之亦然。

练习册系列答案
相关题目
若阿伏加德罗常数的数值为NA,则下列说法中正确的是
| A.1.0L0.1 mol·L-1Na2S溶液中含有的S2-离子数小于0.1NA |
| B.1 molFe与过量的氯气反应,转移电子的数目为2 NA |
| C.2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| D.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
NA表示阿伏加德罗常数,下列叙述正确的是
| A.常温下,9g H2O中含NA个O–H键 |
| B.1 molFe2+与足量稀硝酸反应,转移3 NA个电子 |
| C.常温常压下,22. 4L SO2和O2的混合气体中含2NA个氧原子 |
| D.1 L 0. 1 mol·L-1KAl(SO4)2溶液含0.1NA个Al3+ |
设NA表示阿伏加德罗常数的值,下列说法不正确的是
| A.T0C时,1 L pH=6的纯水中,含有的OH-数目为1×10-6NA |
| B.12.0 g NaHSO4固体中含有的阳离子数目为0.1 NA |
| C.50 g 98%的浓硫酸中,所含的氧原子数目为2NA |
| D.1 molNa2O2与足量CO2充分反应转移的电子数目为NA |
下列化学用语表达正确的是
A.磷原子的原子结构示意图: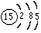 |
B.钠离子的电子式: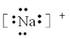 |
C.甲烷的结构式: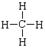 |
| D.质子数为8,中子数为10的核素:10O |
下列各组物质中分子数相同的是( )
| A.2LCO和2LCO2 |
| B.9gH2O和标准状况下11.2LCO2 |
| C.标准状况下1molO2和22.4LH2O |
| D.0.2molH2和4.48LHCl气体 |
加碘盐的主要成分是NaCl,还添加了适量的KIO3。下列说法中正确的是
| A.KIO3和NaCl为离子化合物,均只含离子键 |
B.KIO3中阳离子的结构示意图为 |
| C.23Na37Cl中质子数和中子数之比是8∶7 |
| D.次碘酸的结构式为H—O—I |
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| | 溶质的物质的量浓度/mol·L-1 | 溶液的密度/g·cm-3 |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为________mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与
 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________ c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。 