题目内容
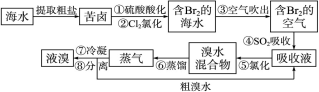
莫尔盐【硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O】是一种重要化学试剂,实验室用含油污的铁片来制取莫尔盐,流程如下:

请回答下列问题:
(1)加入10%Na2CO3溶液的原因是___________________(用离子方程式表示)。
(2)A物质可以为________(填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(3)B物质的成分为_________________。
(4) 加少量硫酸调节pH为 1~2的目的是_____________________________,
操作Ⅱ的名称_______________________________________________。
(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是_________________________________________。
(6)鉴定所得晶体中含有Fe2+、NH 、SO
、SO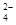 离子的实验方法正确的是________(填编号)。
离子的实验方法正确的是________(填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象

请回答下列问题:
(1)加入10%Na2CO3溶液的原因是___________________(用离子方程式表示)。
(2)A物质可以为________(填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(3)B物质的成分为_________________。
(4) 加少量硫酸调节pH为 1~2的目的是_____________________________,
操作Ⅱ的名称_______________________________________________。
(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是_________________________________________。
(6)鉴定所得晶体中含有Fe2+、NH
 、SO
、SO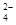 离子的实验方法正确的是________(填编号)。
离子的实验方法正确的是________(填编号)。a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
(1) (2分)CO32— + H2O  HCO3— + OH—
HCO3— + OH—
(2) (2分)b、d
(3)(2分)Fe Cu
(4) (2分)抑制Fe2+、NH4+ 水解; (3分)蒸发浓缩、冷却结晶、过滤
(5) (2分)避免加热过程中晶体受热分解(或被氧化)
(6) (3分)b、c、d
 HCO3— + OH—
HCO3— + OH—(2) (2分)b、d
(3)(2分)Fe Cu
(4) (2分)抑制Fe2+、NH4+ 水解; (3分)蒸发浓缩、冷却结晶、过滤
(5) (2分)避免加热过程中晶体受热分解(或被氧化)
(6) (3分)b、c、d
试题分析:(1)加入10%Na2CO3溶液的目的是去掉油污,碳酸钠水解显碱性,方程式为CO32— + H2O
 HCO3— + OH—;(2)加入的A物质不可以含有氯离子或硝酸根离子,因为这样会引入新的杂质,故可选用CuO或CuSO4;(3)固体B含有反应生成的Cu和未反应的Fe;(4)加少量硫酸调节pH为 1~2的目的是抑制Fe2+、NH4+ 水解;操作II为蒸发浓缩、冷却结晶、过滤;(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是避免加热过程中晶体受热分解(或被氧化);(6)鉴定所得晶体中含有Fe2+可以选用酸性KMnO4溶液,看是否褪色;检验NH
HCO3— + OH—;(2)加入的A物质不可以含有氯离子或硝酸根离子,因为这样会引入新的杂质,故可选用CuO或CuSO4;(3)固体B含有反应生成的Cu和未反应的Fe;(4)加少量硫酸调节pH为 1~2的目的是抑制Fe2+、NH4+ 水解;操作II为蒸发浓缩、冷却结晶、过滤;(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是避免加热过程中晶体受热分解(或被氧化);(6)鉴定所得晶体中含有Fe2+可以选用酸性KMnO4溶液,看是否褪色;检验NH 用浓NaOH溶液并加热,看湿润的红色石蕊试纸是否变蓝;检验SO
用浓NaOH溶液并加热,看湿润的红色石蕊试纸是否变蓝;检验SO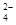 离子可加入盐酸后再加入BaCl2溶液,看是否有白色沉淀产生。
离子可加入盐酸后再加入BaCl2溶液,看是否有白色沉淀产生。
练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目