��Ŀ����
����Ŀ��ԭ���ԭ���ķ����Ǵ��ܺ��ܼ����ľ�������ǻ�ѧ������һ���ش��ס�
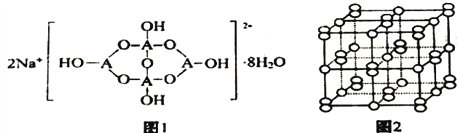
��1����������������Ӧ��A��NaOH + HCl = NaCl + H2O�� B��2FeCl3 + Cu = 2FeCl2 + CuCl2
�ж��ܷ���Ƴ�ԭ���A��__________B��____________������������������������
��2����ͭƬ��пƬ������ϡH2SO4��ɵ�ԭ����У���пƬֻ����ԭ��ظ�ʴ��һ��ʱ���ij�缫����3.36L��״���µ����塣
�ٸ�����_________������п������ͭ������
�������ĵ缫��ӦʽΪ__________________________________��
�۲�����Щ���干��ת�Ƶ���_________________mol��
���𰸡� ���� �� п 2H+ +2e- =H2�� 0.3
�������������������1��ԭ��ط�Ӧһ����������ԭ��Ӧ����2����ԭ����л��ý������������������������ӵõ�������������������������Ӧʽ����ת�Ƶ��ӵ����ʵ�����
��������1��ԭ��ط�Ӧһ����������ԭ��Ӧ��NaOH + HCl = NaCl + H2O�Ƿ�������ԭ��Ӧ����A������Ƴ�ԭ�����2FeCl3 + Cu = 2FeCl2 + CuCl2��������ԭ��Ӧ����B����Ƴ�ԭ�����
��2����ԭ����л��ý�����������п��ͭ���ã����Ը�����п���������������ӵõ��������������缫��Ӧʽ��2H+ +2e- =H2����
�������3.36L��״���µ���������ת�Ƶ���xmol
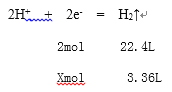
![]()
x=0.3mol

����Ŀ����֪�������ܵ���ʵ��ܶȻ����±���ʾ��
�������ܵ���ʵ�Ksp��25���� | |
�����ܽ�ƽ�� | Ksp |
AgBr(s) | 5,0��10-13 mol2��L-2 |
AgI(s) | 8.3��10-17 mol2��L-2 |
FeS(s) | 6.3��10-18 mol2��L-2 |
ZnS(s) | 1.6��10-24 mol2��L-2 |
CuS(s) | 1.3��10-36 mol2��L-2 |
��1��AgBr��AgI��FeS��ZnS��CuS���ܽ������ɴ�С��˳Ϊ��____________________��
��2���͵�AgI��Һ�м����������������c( I�� )________(����������������С������������)�����ļ�AgBr���壬��c(Ag+)__________(����������������С������������)��
��3����25��ʱ����100mLŨ�Ⱦ�Ϊ0.1 mol��L-1 FeCl2��ZnCl2��CuCl2�Ļ����Һ����μ���Na2S��Һ�����ɵij������Ⱥ�˳����_____________________(�ó�����Ļ�ѧʽ��ʾ)��
��4����25��ʱ����ZnS��������ˮ�У�һ��ʱ���ﵽ����ƽ��: ZnS(s)![]() Zn2+(aq)+S2-(aq)�����д�ʩ��ʹZnS���ٵ��� _______��
Zn2+(aq)+S2-(aq)�����д�ʩ��ʹZnS���ٵ��� _______��
A����������CuS���� B����������FeS����
C����������FeCl2���� D����������CuCl2����