题目内容
16.在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)?xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强).在图中,Y轴是指( )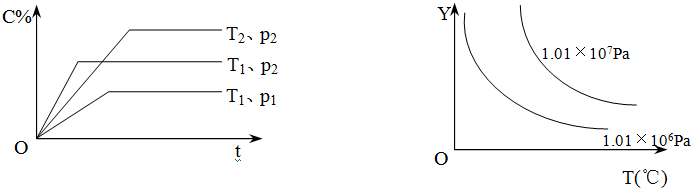
| A. | 反应物A的转化率 | B. | 平衡混合气中物质B的百分含量 | ||
| C. | 平衡混合气的密度 | D. | 该反应的正方向的△H>0 |
分析 根据图1中“先拐先平数值大”知,T1>T2,P2>P1,升高温度,C的含量降低,说明该反应向逆反应方向移动,则正反应是放热反应,增大压强,C的含量增大,平衡向正反应方向移动,则该反应是一个反应前后气体体积减小的反应,即a+b>x,根据化学平衡移动原理来分析即可.
解答 解:根据图1中“先拐先平数值大”知,T1>T2,P2>P1,升高温度,C的含量降低,说明该反应向逆反应方向移动,则正反应是放热反应,增大压强,C的含量增大,平衡向正反应方向移动,则该反应是一个反应前后气体体积减小的反应,即a+b>x;
A.升高温度平衡向逆反应方向移动,则A或B的转化率减小,增大压强平衡正反应方向移动,A或B的转化率增大,符合图象,故A正确;
B.根据图2知,增大压强,平衡向正反应方向移动,则B的体积分数减小,与图象不相符,故B错误;
C.在一定温度下,根据质量守恒知,混合气体的质量始终不变,容器体积不变,则混合气体的密度始终不变,故C错误;
D.根据图1中“先拐先平数值大”知,T1>T2,升高温度,C的含量降低,说明该反应向逆反应方向移动,则正反应是放热反应,△H<0,故D错误;
故选A.
点评 本题考查了温度、压强对化学平衡的影响,根据图1确定该反应的反应热、气体体积系数之间的关系,再结合图2中温度、压强对化学平衡的影响来分析解答,难度中等.

练习册系列答案
相关题目
11.已知下列三个数据:7.1×10-4 mol•L-1、6.8×10-4 mol•L-1、6.2×10-10 mol•L-1分别是三种酸的电离平衡常数.若这三种酸可发生如下反应:
①NaCN+HNO2=HCN+NaNO2 ②NaCN+HF=HCN+NaF ③NaNO2+HF=HNO2+NaF
则下列叙述中不正确的是( )
①NaCN+HNO2=HCN+NaNO2 ②NaCN+HF=HCN+NaF ③NaNO2+HF=HNO2+NaF
则下列叙述中不正确的是( )
| A. | HF的电离平衡常数为7.1×10-4 mol•L-1 | |
| B. | HNO2的电离平衡常数为6.2×10-10 mol•L-1 | |
| C. | 根据①③两个反应即可知三种酸的相对强弱 | |
| D. | HNO2的电离平衡常数比HCN的大,比HF的小 |
8.能用CO32-+2H+=H2O+CO2↑离子方程式表示的反应是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | B. | NaHCO3+HNO3=NaNO3+H2O+CO2↑ | ||
| C. | Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ | D. | BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ |
6.下列说法中正确的是( )
| A. | O2的摩尔质量是16g | |
| B. | 金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物 | |
| C. | 同温、同压下,1mol任何气体所含的气体分子数目都相等 | |
| D. | 标准状况下,体积是22.4升的物质,其物质的量一点是1摩尔 |
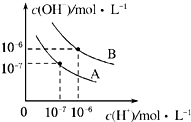 已知水在25℃和95℃时,其电离平衡曲线如图所示.
已知水在25℃和95℃时,其电离平衡曲线如图所示.