题目内容
5.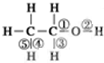 乙醇分子中化学键如图:
乙醇分子中化学键如图:(1)与金属钠反应时,键②断裂;
(2)与浓硫酸共热制乙烯时,键①⑤断裂;
(3)催化氧化为醛时,键②③断裂;
(4)与乙酸发生酯化反应时,键②断裂.
分析 (1)乙醇与金属钠反应生成乙醇钠,脱去羟基上的氢原子;
(2)乙醇发生消去反应生成乙烯,C-OH断裂、与羟基相连碳原子上的C-H断裂;
(2)乙醇的催化氧化,脱去羟基上的氢原子和与羟基相连碳原子上的氢原子;
(3)酯化反应中羧酸提供羧基中羟基,醇提供羟基中H原子,结合生成水,其它基团结合生成酯.
解答 解:(1)乙醇与金属钠反应生成乙醇钠,脱去羟基上的氢原子,②键断裂,故答案为:②;
(2)乙醇发生消去反应生成乙烯,C-OH断裂、与羟基相连碳原子上的C-H断裂,即键①⑤断裂,故答案为:①⑤;
(2)乙醇的催化氧化,脱去羟基上的氢原子和与羟基相连碳原子上的氢原子,键②③断裂,故答案为:②③;
(3)酯化反应中羧酸提供羧基中羟基,醇提供羟基中H原子,结合生成水,其它基团结合生成酯,故乙醇中②键断裂,故答案为:②.
点评 本题考查乙醇的性质,注意根据有机物的结构分析理解化学键断裂与形成,难度不大.

练习册系列答案
相关题目
11.下列有关结构的说法正确的是( )
| A. | 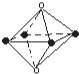 是从NaCl晶体结构图中分割出来的部分结构. 是从NaCl晶体结构图中分割出来的部分结构. | |
| B. | 钡在氧气中燃烧得到一种晶体,其结构如图所示,则该晶体的化学式为Ba2O2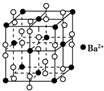 | |
| C. | SiCl4是非极性分子,分子中Si原子处在4个Cl原子所组成的正方形的中心 | |
| D. | 白磷(P4)和甲烷都是正四面体型分子,但分子中的共价键数目和键角均不同 |
16.下列有关化学用语正确的是( )
| A. | HCl的电子式H:Cl | B. | HClO的结构式H-Cl-O | ||
| C. | MgBr2的形成过程用电子式表示为: | D. | Cl-的结构示意图 |
13.已知反应2HBr(g)?Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
下列说法正确的是( )
| 实验序号 | 实验温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.5 | 0.5 | 0.5 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A. | 从上表数据分析,2HBr?Br2+H2正反应为放热反应 | |
| B. | 实验2中HBr的初始浓度C2=1.0 mol/L | |
| C. | 实验3的反应速率小于实验1的反应速率 | |
| D. | 实验4一定使用了催化剂 |
20.下列反应属于吸热反应的是( )
| A. | 氢氧化钡与盐酸溶液反应 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | 石灰石在高温下的分解反应 | D. | 锌粒与稀H2SO4反应制取H2 |
17.A、B、C、D、E、F、G为由七种短周期元素构成的粒子,它们都有10个电子,其结构特点如下表:
其中,B的离子半径大于E的离子半径;D是常温常压下能使湿润红色石蕊试纸变蓝色的气体;C常用作F的检验(加热).请填写下列空白:
(1)A粒子的结构示意图 ,G的化学式是CH4.
,G的化学式是CH4.
(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C反应生成D的离子方程式NH4++OH-=NH3.H2O.
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)A粒子的结构示意图
 ,G的化学式是CH4.
,G的化学式是CH4.(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C反应生成D的离子方程式NH4++OH-=NH3.H2O.
14.已知:
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
| A. | 正丁烷的稳定性大于异丁烷 | |
| B. | 异丁烷分子中的碳氢键比正丁烷的多 | |
| C. | 等物质的量的正丁烷能量大于异丁烷能量 | |
| D. | 异丁烷转化为正丁烷的过程是一个放热过程 |
15.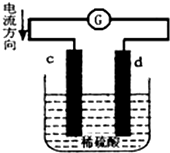 将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
 将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )| A. | 当电路中通过2 mol 电子时,d 极可以生成22.4 L H2 | |
| B. | 当电路中通过0.1 mol 电子时,溶液中c(Zn2+)=0.5 mol•L-1 | |
| C. | c为负极,发生氧化反应 | |
| D. | 电池工作完成后,溶液中SO42-浓度基本不变 |
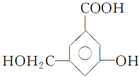
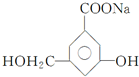 、
、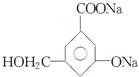 、
、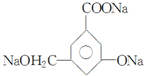 .
.