题目内容
常温下,0.1 mol·L-1某一元酸HA溶液中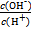 =1×10-12,下列说法中正确的是
=1×10-12,下列说法中正确的是
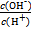 =1×10-12,下列说法中正确的是
=1×10-12,下列说法中正确的是| A.溶液中由水电离出的c(H+)=1×10-10 mol·L-1 |
B.溶液中存在HA H++A- H++A- |
| C.与0.1 mol·L-1 NaOH溶液等体积混合后所得溶液为中性 |
| D.原溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大 |
C
结合KW=10-14可计算出溶液中c(H+)=1×10-1 mol·L-1、c(OH-)=1×10-13mol·L-1,所以HA是强酸,B、D选项错误,C选项正确;溶液中的c(OH-)就等于水电离出的c(OH-)=1×10-13mol·L-1,所以水电离出的c(H+)=1×10-13 mol·L-1,A选项错误。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
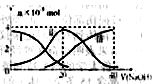
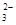
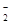
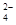
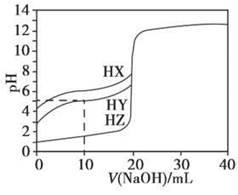
 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)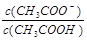 <1
<1 H2(g)+
H2(g)+