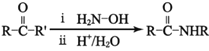题目内容
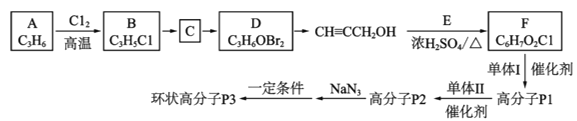
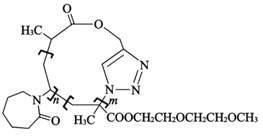
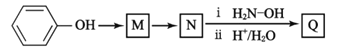
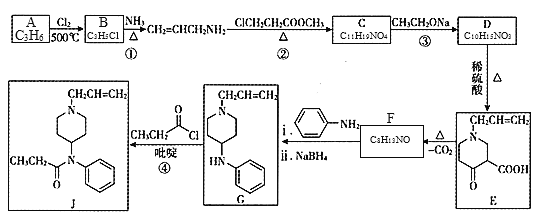
【题目】镇痛药物J的合成方法如下:
已知:
![]() +Cl-R3
+Cl-R3![]()
![]() +HCl
+HCl
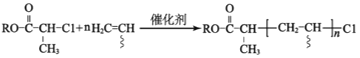
R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
![]()
![]()
![]()
(R1、R2、R3、R4为氢或烃基)
(1)B的名称为______;F的结构简式为______。
(2)C中含氧官能团名称为______;②的反应类型为______反应。
(3)③的化学方程式为______。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有______种。
A.遇FeCl3显紫色 B.苯环上有三个取代基
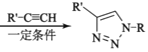
(5)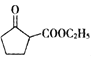 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出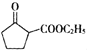 的合成路线______。(已知:RHC=CHR
的合成路线______。(已知:RHC=CHR![]() RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
【答案】3-氯丙烯 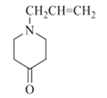 酯基 取代
酯基 取代 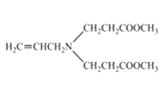
![]()
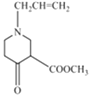 +CH3OH 30
+CH3OH 30 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
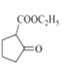
【解析】
由框图![]() 可知A为CH3CH=CH2,A到B发生取代反应,B的结构简式为CH2ClCH=CH2;由框图
可知A为CH3CH=CH2,A到B发生取代反应,B的结构简式为CH2ClCH=CH2;由框图![]() 可知发生了取代反应,根据
可知发生了取代反应,根据![]() +Cl-R3
+Cl-R3![]()
![]() +HCl可知生成的C的结构简式为
+HCl可知生成的C的结构简式为![]() ,由
,由![]() 可知,③发生反应的方程式为:
可知,③发生反应的方程式为: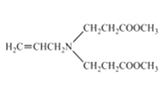
![]()
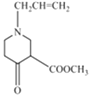 +CH3OH,生成的D的结构简式
+CH3OH,生成的D的结构简式  在硫酸作用下加热发生水解反应生成E,E的结构简式为
在硫酸作用下加热发生水解反应生成E,E的结构简式为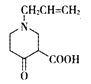 ,再通过
,再通过 得到F,则F的结构简式为
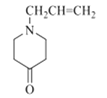 ;然后依次发生取代反应生成G、J;
;然后依次发生取代反应生成G、J;
(6)以环已醇![]() 和乙醇为起始原料合成
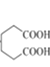
和乙醇为起始原料合成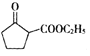 ,环己醇发生消去反应生成环己烯,环己烯发生氧化反应生成己二酸,己二酸发生酯化反应生成己二酸二乙酯,然后发生信息反应生成
,环己醇发生消去反应生成环己烯,环己烯发生氧化反应生成己二酸,己二酸发生酯化反应生成己二酸二乙酯,然后发生信息反应生成 。
。
(1)根据上述分析B的结构简式为![]() ,则B的名称为3-氯丙烯(或3-氯-1-丙烯);F的结构简式为
,则B的名称为3-氯丙烯(或3-氯-1-丙烯);F的结构简式为 ,故答案为:3-氯丙烯(或3-氯-1-丙烯);
,故答案为:3-氯丙烯(或3-氯-1-丙烯); ;
;
(2) 根据上述分析C的结构简式为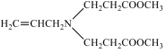 ,C中含氧官能团名称为酯基;②的反应类型为取代反应,故答案为:酯基;取代;
,C中含氧官能团名称为酯基;②的反应类型为取代反应,故答案为:酯基;取代;
(3) 根据上述分析可知:③的化学方程式为
![]()
 +CH3OH,
+CH3OH,
故答案为:
![]()
 +CH3OH;
+CH3OH;
(4) 根据上述分析F的结构简式为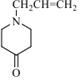 ,有机物K分子组成比F少两个氢原子,K的同分异构体符合下列条件,A.遇
,有机物K分子组成比F少两个氢原子,K的同分异构体符合下列条件,A.遇![]() 显紫色,说明含有酚羟基;B.苯环上有三个取代基,F的不饱和度是3,K的不饱和度是4,苯环的不饱和度是4,所以K的同分异构体中除了苯环外不含其它双键或三键,如果取代基为
显紫色,说明含有酚羟基;B.苯环上有三个取代基,F的不饱和度是3,K的不饱和度是4,苯环的不饱和度是4,所以K的同分异构体中除了苯环外不含其它双键或三键,如果取代基为![]() 、
、![]() 、
、![]() ,有10种,如果取代基为
,有10种,如果取代基为![]() 、
、![]() 、
、![]() ,有10种;如果取代基为
,有10种;如果取代基为![]() 、
、![]() 、
、![]() ,有10种,所以符合条件的同分异构体种类是30种,故答案为:30;
,有10种,所以符合条件的同分异构体种类是30种,故答案为:30;
(5)以环已醇(![]() )和乙醇为起始原料合成
)和乙醇为起始原料合成 ,环己醇发生消去反应生成环己烯,环己烯发生氧化反应生成己二酸,己二酸发生酯化反应生成己二酸二乙酯,然后发生信息反应生成
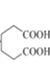
,环己醇发生消去反应生成环己烯,环己烯发生氧化反应生成己二酸,己二酸发生酯化反应生成己二酸二乙酯,然后发生信息反应生成 ,其合成路线为
,其合成路线为![]()
![]()
![]()
![]()
![]()
![]()
![]()
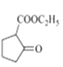 ,故答案为:
,故答案为:![]()
![]()
![]()
![]()

![]()
![]()
![]()
 。
。

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案