题目内容
【题目】一种三室微生物燃料电池污水净化系统原理如右图所示。图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是
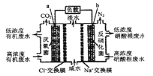
A.b电极为该电池的负极
B.b电极附近溶液的pH减小
C.a电极反应式:C6H10O5-24e-+7H2O═6CO2↑+24H+
D.中间室:Na+移向左室,Cl-移向右室
【答案】C
【解析】
试题分析:该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+;A.该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,故A错误;B.右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,氢离子参加反应导致溶液酸性减小,溶液的pH增大,故B错误;C.左边装置电极a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+,故C正确;D.放电时,电解质溶液中阳离子Na+移向正极右室,阴离子Cl-移向负极室左室,故D错误;故选C。

【题目】二甲醚(CH3OCH3)是一种新型能源,利用二氧化碳合成新能源已成为环保化学家研究的热门课题。
(1)几种共价键的键能如表所示:
化学键 | C=O | H-H | C-H | C-O | H-O |
键能/kJ·mol-1 | 803 | 436 | 414 | 326 | 464 |
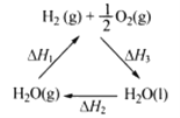
2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ![]() _______________。
_______________。
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料。科研人员模拟光合作用,设计如图甲所示装置制备二甲醚。能量转化形式为太阳能![]() 电能
电能![]() 化学能、
化学能、
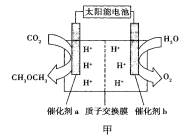
①催化剂b的电极名称是_________________。
②若释放11.2L氧气(标准状况下),有___________mol H+___________(填质子的迁移方向)。
③催化剂a上的电极反应式为______________。
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
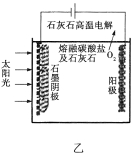
①生产过程中能量的转化形式是__________________。
②电解反应在温度小于900![]() 时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。
时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。