题目内容
3.下列各组离子能在指定溶液中大量共存的是( )| A. | 无色溶液中:K+、Cl-、NH4+、AlO2-、SO42- | |
| B. | 常温下,pH=14的溶液中:CO32-、Na+、S2-、AlO2- | |
| C. | 室温下,水电离出的c(OH-)=10-13mol•L-1的溶液中:K+、HCO3-、Br-、Ba2+ | |
| D. | 使甲基橙变红的溶液中:Fe2+、Al3+、I-、NO3- |
分析 A.铵根离子与偏铝酸根离子发生双水解反应;
B.该溶液为碱性溶液,四种离子之间不反应,都不与碱性溶液中的氢氧根离子反应;
C.室温下,水电离出的c(OH-)=10-13mol•L-1的溶液为酸性或碱性溶液,碳酸氢根离子能够与酸性和碱性溶液反应;
D.使甲基橙变红的溶液为酸性溶液,硝酸根离子在酸性条件下能够氧化碘离子、亚铁离子.
解答 解:A.NH4+、AlO2-之间发生双水解反应生成氢氧化铝沉淀,在溶液中不能大量共存,故A错误;
B.常温下pH=14的溶液为碱性溶液,溶液中存在大量氢氧根离子,CO32-、Na+、S2-、AlO2-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.室温下,水电离出的c(OH-)=10-13mol•L-1的溶液中存在大量氢离子或奇异果干离子,HCO3-能够与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.该溶液为酸性溶液,NO3-在酸性条件下具有强氧化性,能够氧化Fe2+、I-,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
9.如图类似于教材P14关于验证“氯气的漂白性实验”的装置图.但在实验时,某同学将A、B两装置的先后位置交换了,则该同学可能看到的实验现象是( )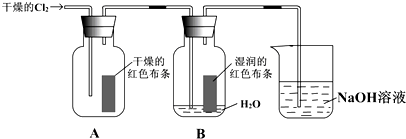

| A. | 只有干燥的布条褪色 | B. | 只有湿润的布条褪色 | ||
| C. | 两块布条均褪色 | D. | 两块布条均不褪色 |
11.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Na2O2 溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 大理石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
13.下列过程属于氮的固定的是( )
| A. | N2和H2在一定条件下合成氨 | B. | 由氨制成硫酸铵 | ||
| C. | NO和O2反应生成NO2 | D. | NO2与H2O反应 |
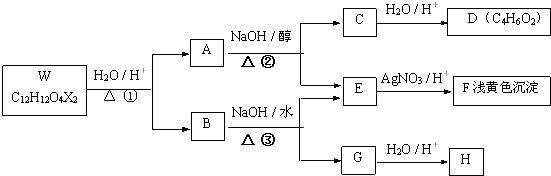

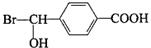
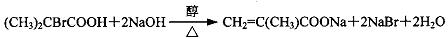
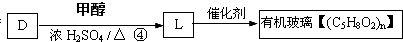 ,反应④的化学方程式是
,反应④的化学方程式是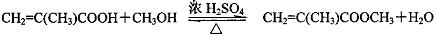
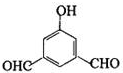 、
、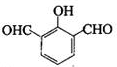 、
、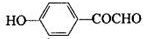 .
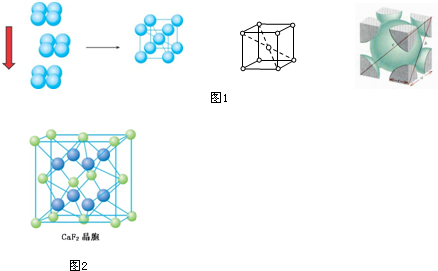
.
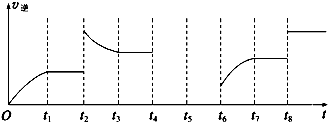
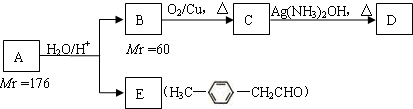 烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3:4.与A相关的反应如下
烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3:4.与A相关的反应如下 ;
;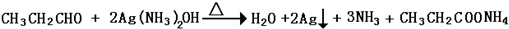 ;
; 、
、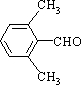 、
、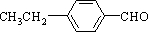 任意2种.(任写其中二种就可)
任意2种.(任写其中二种就可)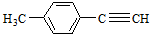 )的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任选).合成路线流程图示例如下: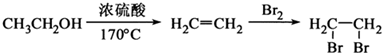
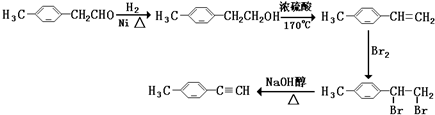
 .
.