题目内容
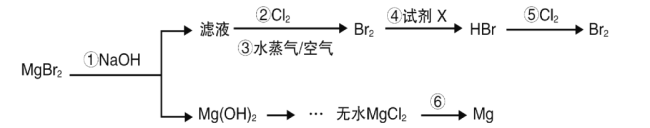
【题目】海水是巨大的资源宝库,从海水中可以提取镁、溴等产品。某兴趣小组以MgBr2为原料,模拟从海水中制备溴和镁。下列说法错误的是( )
A.工业上步骤①常用Ca(OH)2代替NaOH
B.设计步骤②、③、④的目的是为了富集溴
C.步骤④中试剂X可选用饱和二氧化硫水溶液
D.工业上实现步骤⑥,通常用氢气还原氯化镁
【答案】D
【解析】
由流程可知,MgBr2与NaOH反生成氢氧化镁和NaBr,则滤液含NaBr,②中氯气可氧化溴离子生成溴,③吹出溴,④中试剂X为二氧化硫的水溶液,可吸收溴并生成HBr,⑤中氯气与HBr反应生成溴;氢氧化镁与盐酸反应生成MgCl2溶液,蒸发浓缩、冷却结晶得到MgCl26H2O,在HCl气流中加热MgCl26H2O,使其脱去结晶水得到无水MgCl2,⑥中电解熔融MgCl2生成Mg,以此来解答。
A. 工业上步骤①常用Ca(OH)2代替NaOH,便宜易得,故A正确;
B. 海水中溴离子浓度较低,步骤②、③、④的目的是为了富集溴,故B正确;
C. 步骤④中试剂X可选用饱和二氧化硫水溶液,与溴单质发生氧化还原反应SO2+Br2+2H2O=H2SO4+2HBr,生成HBr,故C正确;
D. Mg为活泼金属,其还原性强于氢气,氢气无法还原氯化镁,工业上实现步骤⑥,通常用电解法,故D错误;
故选D。

练习册系列答案
相关题目