题目内容
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应:N2(g)+3H2(g)![]() 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
A.v(H2)=0.2mol·L-1·min-1
B.v(N2)=0.2 mol·L-1·min-1
C.v(N2)=0.02 mol·L-1·s-1
D.v(H2)= 0.04 mol·L-1·s-1
【答案】C
【解析】
试题分析:都用氮气的浓度变化表示化学反应速率,并且单位一致,然后再进行比较。A.v(H2)=0.2mol·L-1·min-1,则v(N2)=1/3 v(H2)=0.067 mol·L-1·min-1 ;B.v(N2)=0.2 mol·L-1·min-1;C.v(N2)=0.02 mol·L-1·s-1,用mol·L-1·min-1表示速率单位是v(N2)=1.2 mol·L-1·min-1;D.v(H2)= 0.04 mol·L-1·s-1,用mol·L-1·min-1表示速率单位,则v(N2)= (0.04×60)÷3=0.8 mol·L-1·min-1,可见产生氨气速率最快的是选项C。

 阅读快车系列答案
阅读快车系列答案【题目】实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH![]() CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
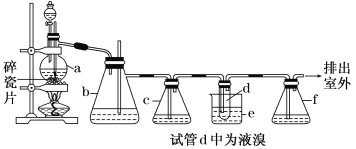
有关数据列表如下:
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是______________________。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是______________________; 但不用冰水进行过度冷却,原因_______________________________________________。
【题目】下表是生活生产中常见的物质,表中列出了它们的(主要)成分
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
名称 | 酒 精 | 醋酸 | 火碱 | 食盐 | 铜线 | 氨气 | 苏打 | 小苏打 |
主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | NH3 | Na2CO3 | NaHCO3 |
根据情景回答问题
(1)请你对表中①~的主要成分进行分类:属于电解质的是____________(填编号)
(2)写出⑧的主要成分溶于水的电离方程式_______________________________
(3)写出NaHCO3受热分解的化学方程式_______________________________