ĖâÄŋÄÚČÝ
1ĢŪÐīģöÏÂÁзīÓĶĩÄČČŧŊŅ§·―ģĖĘ―ĢĻ1ĢĐÔÚ25ĄæĢŽ101Kpa ÏÂ1mol ŌŌīžĢĻC2H5OHĢĐÍęČŦČžÉÕēĒÉúģÉķþŅõŧŊĖžšÍŌšĖŽËŪĘąĢŽ·ÅģöČČÁŋΊ1366.8kJĢŽĘÔÐīģöąíĘūŌŌīžČžÉÕĩÄČČŧŊŅ§·―ģĖĘ―ĢšC2H5OHĢĻlĢĐ+3O2ĢĻgĢĐĻT2CO2ĢĻgĢĐ+3H2OĢĻlĢĐĄũH=-1366.8 kJ•mol-1
ĢĻ2ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔŌšĖåĢŽÆäČžÉÕČČ―ÏīóĮŌČžÉÕēúÎïķÔŧ·ūģÎÞÎÛČūĢŽđĘŋÉŌÔÓÃŨũŧðžýČžÁÏĢŪŌŅÖŠĢšN2ĢĻgĢĐ+2O2 ĢĻgĢĐĻT2NO2ĢĻgĢĐĄũH=+67.7kJ/mol
2N2H4ĢĻgĢĐ+2NO2ĢĻgĢĐĻT3N2ĢĻgĢĐ+4H2OĢĻgĢĐĄũH=Ōŧ1135.7kJ/mol
ÔōëÂÍęČŦČžÉÕĩÄČČŧŊŅ§·―ģĖĘ―ÎŠN2H4ĢĻlĢĐ+O2ĢĻgĢĐ=N2ĢĻgĢĐ+2H2OĢĻlĢĐĄũH=-534kJ/molĢŪ
ĢĻ3ĢĐļßÂŊÁķĖúÖзĒÉúĩÄŧųąū·īÓĶÖŪŌŧČįÏÂĢšFeOĢĻsĢĐ+COĢĻgĢĐĻTFeĢĻsĢĐ+CO2ĢĻgĢĐĄũHĢū0ĢŪ
ĒŲīË·īÓĶĩÄÆ―šâģĢĘýąíīïĘ―ÎŠ$\frac{cĢĻC{O}_{2}ĢĐ}{cĢĻCOĢĐ}$Ģŧ
ĒÚÎÂķČÉýļßÆ―šâģĢĘýKÖĩÔöīó ĢĻĖÔöī󥹥ĒĄ°žõÐĄĄąĄĒŧōĄ°ēŧąäĄąĢĐ
ĒÛŌŅÖŠ1100ĄæĘąĢŽK=0.263ĢŽīËĘąēâĩÃļßÂŊÖÐcĢĻCO2ĢĐ=0.025mol/LĢŽcĢĻCOĢĐ=0.1mol/LĢŽÔÚÕâÖÖĮéŋöÏÂĢŽļ÷īÓĶēŧĘĮĢĻĖĘĮĄąŧōĄ°ēŧĘĮĄąĢĐīĶÓÚŧŊŅ§Æ―šâŨīĖŽĢŽīËĘąŧŊŅ§·īÓĶËŲÂĘĘĮvÕýĢū vÄæĢĻĖĢžĄąĄĒĄ°ĢūĄąŧōĄ°=ĄąĢĐĢŪ
·ÖÎö ĢĻ1ĢĐŌĀūÝČžÉÕČČĩÄķĻŌå―âīðĢŽąíĘūČžÉÕČČĩÄČČŧŊŅ§·―ģĖĘ―ÖÐŋÉČžÎïΊ1molĢŽēúÎïΊÎČķĻŅõŧŊÎïĢŧŌĀūÝ1mol ŌŌīžĢĻC2H5OHĢĐÍęČŦČžÉÕēĒÉúģÉķþŅõŧŊĖžšÍŌšĖŽËŪĘąĢŽ·ÅģöČČÁŋΊ1366.8kJĢŽÐīģöČČŧŊŅ§·―ģĖĘ―Ģŧ
ĢĻ2ĢĐŌĀūÝČČŧŊŅ§·―ģĖĘ―šÍļĮËđķĻÂÉžÆËãĩÃĩ―ĢĻĒŲ+ĒÚĢĐĄÁ$\frac{1}{2}$ĩÃĩ―N2H4ĢĻlĢĐ+O2ĢĻgĢĐ=N2ĢĻgĢĐ+2H2OĢĻlĢĐĢŽūÝīËžÆËãėĘąäĢŧ
ĢĻ3ĢĐĒŲŧŊŅ§Æ―šâģĢĘýÖļÔÚŌŧķĻÎÂķČÏÂĢŽŋÉÄæ·īÓĶķžīïĩ―Æ―šâĘąļũÉúģÉÎïÅĻķČĩÄŧŊŅ§žÆÁŋĘýīÎÃÝĩÄģËŧýģýŌÔļũ·īÓĶÎïÅĻķČĩÄŧŊŅ§žÆÁŋĘýīÎÃÝĩÄģËŧýËųĩÃĩÄąČÖĩĢŽđĖĖåĄĒīŋŌšĖåēŧÐčŌŠąíĘūģöĢŧ
ĒÚļ÷īÓĶÕý·īÓĶĘĮÎüČČ·īÓĶĢŽÎÂķČÉýļßÆ―šâÏōÕý·īÓĶ·―ÏōŌÆķŊĢŽūÝīËÅÐķÏĢŧ
ĒÛžÆËãīËĘąĩÄÅĻķČÉĖQcĢŽÓëÆ―šâģĢĘýąČ―ÏÅÐķÏ·īÓĶ―øÐз―ÏōĢŪ
―âīð ―âĢšĢĻ1ĢĐČžÉÕČČĘĮÖļĢšÔÚ25ĄæĄĒ101KPaĘąĢŽ1molīŋūŧÎïÍęČŦČžÉÕÉúģÉÎČķĻĩÄŅõŧŊÎï·ÅģöĩÄČČÁŋĢŧ
1mol ŌŌīžĢĻC2H5OHĢĐÍęČŦČžÉÕēĒÉúģÉķþŅõŧŊĖžšÍŌšĖŽËŪĘąĢŽ·ÅģöČČÁŋΊ1366.8kJĢŽÆäČžÉÕČČĩÄČČŧŊŅ§·―ģĖĘ―ÎŠĢšC2H5OHĢĻlĢĐ+3O2ĢĻgĢĐĻT2CO2ĢĻgĢĐ+3H2OĢĻlĢĐĄũH=-1366.8 kJ•mol-1Ģŧ
đĘīð°ļΊĢšC2H5OHĢĻlĢĐ+3O2ĢĻgĢĐĻT2CO2ĢĻgĢĐ+3H2OĢĻlĢĐĄũH=-1366.8 kJ•mol-1Ģŧ
ĢĻ2ĢĐĒŲN2ĢĻgĢĐ+2O2ĢĻgĢĐ=2NO2ĢĻgĢĐĄũH=+67.7kJ/mol
ĒÚ2N2H4ĢĻlĢĐ+2NO2ĢĻgĢĐ=3N2ĢĻgĢĐ+4H2OĢĻlĢĐĄũH=-1135.7kJ/mol
―ášÏļĮËđķĻÂÉžÆËãĢĻĒŲ+ĒÚĢĐĄÁ$\frac{1}{2}$ĩÃĩ―N2H4ĢĻlĢĐ+O2ĢĻgĢĐ=N2ĢĻgĢĐ+2H2OĢĻlĢĐĄũH=-534kJ/molĢŽ
đĘīð°ļΊĢšN2H4ĢĻlĢĐ+O2ĢĻgĢĐ=N2ĢĻgĢĐ+2H2OĢĻlĢĐĄũH=-534kJ/molĢŧ
ĢĻ3ĢĐĒŲŋÉÄæ·īÓĶFeOĢĻsĢĐ+CO ĢĻgĢĐ?FeĢĻsĢĐ+CO2ĢĻgĢĐĩÄÆ―šâģĢĘýąíīïĘ―k=$\frac{cĢĻC{O}_{2}ĢĐ}{cĢĻCOĢĐ}$ĢŽđĘīð°ļΊĢš$\frac{cĢĻC{O}_{2}ĢĐ}{cĢĻCOĢĐ}$Ģŧ
ĢĻ2ĢĐļ÷īÓĶÕý·īÓĶĘĮÎüČČ·īÓĶĢŽÎÂķČÉýļßÆ―šâÏōÕý·īÓĶ·―ÏōŌÆķŊĢŽCO2ĩÄÎïÖĘĩÄÁŋÔöīóĄĒCOĩÄÎïÖĘĩÄÁŋžõÐĄĢŽđĘĩ―īïÐÂÆ―šâĘĮCO2ÓëCOĩÄĖåŧýÖŪąČÔöīóĢŽ
đĘīð°ļΊĢšÔöīóĢŧ
ĢĻ3ĢĐīËĘąÅĻķČÉĖQc=$\frac{0.025}{0.1}$=0.25ĢŽÐĄÓÚÆ―šâģĢĘý2.63ĢŽđĘ·īÓĶēŧĘĮÆ―šâŨīĖŽĢŽ·īÓĶÏōÕý·īÓĶ―øÐÐĢŽÕý·īÓĶËŲÂĘīóÓÚÄã·īÓĶËŲÂĘĢŽ
đĘīð°ļΊĢšēŧĘĮĢŧĢūĢŪ
ĩãÆĀ ąūĖâŋžēéÁËČžÉÕČČĩÄļÅÄîŌÔž°ČžÉÕČČĩÄČČŧŊŅ§·―ģĖĘ―ĩÄĘéÐīŌÔž°ļĮËđķĻÂÉĩÄÓĶÓÃĢŽŧŊŅ§Æ―šâģĢĘýĩÄĘéÐīÓëÔËÓÃĄĒŧŊŅ§Æ―šâÓ°ÏėŌōËØĩČĢŽŨĒŌâČžÉÕČČĩÄČČŧŊŅ§·―ģĖĘ―ÖÐŋÉČžÎïĩÄÎïÖĘĩÄÁŋΊ1molĢŽēúÎïąØÐëĘĮÎČķĻĩÄŅõŧŊÎïĢŽÄŅķČÖÐĩČĢŽēāÖØķÔŧųīĄÖŠĘķĩÄđŪđĖÓëÔËÓÃĢŽŨĒŌâÕÆÎÕŧŊŅ§Æ―šâģĢĘýĩÄĘéÐīÓëÓĶÓÃĢŪ

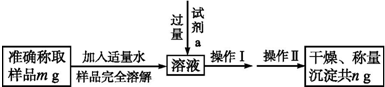
 ČįÍžËųĘūĢŽÁ―ÔēČĶÏā―ŧŌõÓ°ēŋ·ÖąíĘūÔēČĶÄÚÎïÖĘÏāŧĨ·ĒÉúĩÄ·īÓĶĢŪÄÆž°ÆäŅõŧŊÎïĩÄÎïÖĘĩÄÁŋūųΊ0.1molČÜÓÚËŪĢŽÐÎģÉ1LČÜŌšĢŪÏÂÁÐËĩ·ĻÕýČ·ĩÄĘĮĢĻĄĄĄĄĢĐ
ČįÍžËųĘūĢŽÁ―ÔēČĶÏā―ŧŌõÓ°ēŋ·ÖąíĘūÔēČĶÄÚÎïÖĘÏāŧĨ·ĒÉúĩÄ·īÓĶĢŪÄÆž°ÆäŅõŧŊÎïĩÄÎïÖĘĩÄÁŋūųΊ0.1molČÜÓÚËŪĢŽÐÎģÉ1LČÜŌšĢŪÏÂÁÐËĩ·ĻÕýČ·ĩÄĘĮĢĻĄĄĄĄĢĐ| AĢŪ | žŨĄĒŌŌĄĒąûķžĘôÓÚŅõŧŊŧđÔ·īÓĶ | |
| BĢŪ | žŨ·īÓĶĩÄĀëŨÓ·―ģĖĘ―ÎŠNa+2H2OĻTNa++2OH-+H2Ąü | |
| CĢŪ | ąûģä·Ö·īÓĶĢŽÄÜēúÉú0.05 mol O2ĢŽŨŠŌÆĩįŨÓ0.1 mol | |
| DĢŪ | žŨĄĒŌŌĄĒąûģä·Ö·īÓĶšóËųĩÃČÜŌšĩÄÎïÖĘĩÄÁŋÅĻķČΊC1ĄĒC2ĄĒC3ĢŽÔōC1=C2=C3 |
| AĢŪ | ËÄÂČŧŊĖž | BĢŪ | ūÆūŦ | CĢŪ | ÆûÓÍ | DĢŪ | ÂČŧŊÄÆČÜŌš |
| AĢŪ | žÓČëÉŲÁŋNaOHđĖĖåĢŽČÜŌšÖÐcĢĻOH-ĢĐžõÉŲ | |
| BĢŪ | ÍĻČëÉŲÁŋHClÆøĖåĢŽÆ―šâÕýÏōŌÆķŊ | |
| CĢŪ | žÓËŪĢŽ·īÓĶËŲÂĘÔöīóĢŽÆ―šâÄæÏōŌÆķŊ | |
| DĢŪ | žÓČëÉŲÁŋNH4ClđĖĖåĢŽÆ―šâÕýÏōŌÆķŊ |
| ŌŅÖŠ | ĀāÍÆ | |
| A | ―ŦFežÓČëCuSO4ČÜŌšÖÐ Fe+Cu2+=Cu+Fe2+ | ―ŦNažÓČëĩ―CuSO4ČÜŌšÖÐ 2Na+Cu2+=Cu+2Na+ |
| B | ÏōīÎÂČËáļÆČÜŌšÖÐÍĻČëķþŅõŧŊĖžÆøĖå Ca2++2ClO-+CO2+H2O=CaCO3Ąý+2HClO | ÏōīÎÂČËáļÆČÜŌšÖÐÍĻČëķþŅõŧŊÁōÆøĖå Ca2++2ClO-+SO2+H2O=CaSO3Ąý+2HClO |
| C | ÓÃķčÐÔĩįžŦĩį―âCuSO4ČÜŌš 2Cu2++2H2O$\frac{\underline{\;ĩį―â\;}}{\;}$2Cu+O2Ąü+4H- | ÓÃķčÐÔĩįžŦĩį―âCuCl2ČÜŌš 2Cu2++2H2O$\frac{\underline{\;ĩį―â\;}}{\;}$2Cu+O2Ąü+4H- |
| D | ―ŦÉŲÁŋCaCO3·ÛÄĐÍķČëŨãÁŋŅÎËáÖÐ CaCO3+2H+ĻTCa2++CO2Ąü+H2O | ―ŦÉŲÁŋCaCO3·ÛÄĐÍķČëŨãÁŋÏõËáČÜŌšÖÐ CaCO3+2H+ĻTCa2++CO2Ąü+H2O |
| AĢŪ | A | BĢŪ | B | CĢŪ | C | DĢŪ | D |