题目内容
16.25℃时,用0.100mol/L NaOH 溶液分别滴定20.00mL 0.100mol/L的盐酸和20.00mL 0.100mol/L醋酸(忽略温度变化).下列说法正确的是( )| A. | 滴定前,盐酸和醋酸溶液中:c(Cl?)<c(CH3COO-) | |
| B. | 分别加入10.00 mL NaOH溶液时,测得醋酸反应后所得溶液pH=6,则溶液中c(CH3COO−)c(CH3COOH)>1 | |
| C. | 当两种溶液的pH均等于7时,两种酸所消耗NaOH溶液体积不相等,醋酸消耗的NaOH溶液体积多 | |
| D. | 加入20.00 mL NaOH溶液时,所得两种溶液中:c(Cl?)<c(CH3COO-) |
分析 A.根据盐酸和醋酸的电离程度来判断判断;
B.醋酸电离大于醋酸根的水解程度;
C.醋酸钠水解呈碱性;
D.V(NaOH)=20.00 mL 时,二者反应生成氯化钠和醋酸钠.
解答 解:A.盐酸完全电离,滴定前0.100mol/L盐酸中c(Cl?)=0.100mol/L,醋酸属于弱电解质,部分电离,故c(CH3COO-)<0.100mol/L,故A错误;
B.加入10ml氢氧化钠时,溶液中恰好为同浓度的醋酸和醋酸钠,溶液pH=6,说明醋酸电离大于醋酸根的水解程度,故此时,c(CH3COO−)c(CH3COOH)>1,故B正确;
C.醋酸钠水解呈碱性,氯化钠不水解,pH=7时,醋酸所用NaOH溶液的体积小,故C错误;
D.V(NaOH)=20.00 mL 时,二者反应生成氯化钠和醋酸钠,醋酸根发生水解,浓度小于氯离子,故D错误,故选B.
点评 本题考查NaOH与CH3COOH、盐酸的反应,涉及盐类的水解和溶液离子浓度的大小比较知识,注意利用醋酸电离大于醋酸根的水解程度做题.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
4.一定温度下,可逆反应A(气)+3B(气)?2C(气)在一定容积的密闭容器中进行,达到平衡的标志是( )
| A. | 混合气体的密度不再变化 | B. | A、B、C的浓度相等 | ||
| C. | 混合气体的压强不再变化 |
11.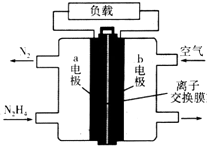 液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )
 液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )| A. | a极的反应式:N2H4+4OH--4e-═N2↑+4H2O | |
| B. | 放电时,电子从a极经过负载流向b极 | |
| C. | 该电池持续放电时,离子交换膜需选用阴离子交换膜 | |
| D. | 电路中转移电子3NA时消耗氧气16.8 L |
1.关于烷烃的叙述不正确的是( )
| A. | 分子式符合CnH2n+2的烃一定是烷烃 | |
| B. | 烷烃均能与氯水发生取代反应 | |
| C. | 辛烷的熔沸点比壬烷低 | |
| D. | 烷烃不能被酸性高锰酸钾等强氧化剂氧化 |
8.下列区分苯和己烯的试验方法和判断正确的是( )
| A. | 分别点燃,无黑烟生成的是苯 | |
| B. | 分别加入溴水振荡,静置后分层,橙黄色消失的是己烯 | |
| C. | 分别加入溴的CCl4,静置后分层,上下两层均为无色的是已烯 | |
| D. | 分别加入酸性KMnO4溶液振荡,紫色消失的是己烯 |
5.下列有关油脂的叙述不正确的是( )
①油脂是高级脂肪酸和甘油所生成的酯
②油脂属于酯类
③油脂都能发生氢化反应
④某油脂分子中,所含烃基有三种,但每一个油脂分子中所含的三种烃基都相同,而且排列结构也相同,则该油脂为混合物
⑤天然油脂没有固定的熔点和沸点,所以天然油脂是混合物.
①油脂是高级脂肪酸和甘油所生成的酯
②油脂属于酯类
③油脂都能发生氢化反应
④某油脂分子中,所含烃基有三种,但每一个油脂分子中所含的三种烃基都相同,而且排列结构也相同,则该油脂为混合物
⑤天然油脂没有固定的熔点和沸点,所以天然油脂是混合物.
| A. | ①② | B. | ②④ | C. | ③④ | D. | ④⑤ |
6.下列说法不正确的是( )
| A. | Na与H2O的反应是熵增的放热反应,该反应能自发进行 | |
| B. | 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 | |
| C. | FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 | |
| D. | Mg(OH)2固体在溶液存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |

 .
. .
.
 +H2O.
+H2O.