题目内容
【题目】光刻胶是一种应用广泛的光敏材料,其合成路线如下(部分试剂、反应条件和产物已略去):

已知:I、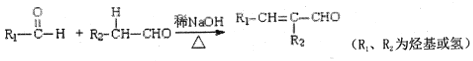
II、
(1)A分子的名称为______,B分子中所含官能团的名称为_______,由C到D的反应类型为_______;
(2)乙炔和羧酸X发生加成反应生成E,E的核磁共振氢谱有三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为_______;
(3)D和G反应生成光刻胶的化学方程式为______;
(4)C的同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②分子中只有一个环状结构。满足上述条件的同分异构体有______种。其中苯环上的一氯取代产物只有两种的同分异构体的结构简式为:_______
(5)根据已有知识并结合本题信息,写出以 CH3CHO为原料制备CH3COCOCOOH的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)______。
【答案】苯甲醛 碳碳双键和醛基 取代反应 ![]()
 3种
3种 ![]()

【解析】
由题给信息可推出A的分子式C7H6O,为苯甲醛,B为![]() , C为
, C为![]() ,E为
,E为![]() 。
。
(1)A分子的名称为苯甲醛,B为![]() ,所含官能团的名称为碳碳双键和醛基, C为
,所含官能团的名称为碳碳双键和醛基, C为![]() ,发生取代反应生成D,故答案为:苯甲醛;碳碳双键和醛基;取代反应。
,发生取代反应生成D,故答案为:苯甲醛;碳碳双键和醛基;取代反应。
(2)乙炔和羧酸X发生加成反应生成E,E发生加聚反应得到F,则E中含有碳碳双键,
结合分子式可知,X为CH3COOH,E的核磁共振氢谱有三组峰,且峰面积比为3:2:1,E能发生水解反应,故E为CH3COOCH=CH2,故答案为:CH3COOCH=CH2。
(3)D和G发生信息II的反应得到光刻胶,化学方程式为
 ,故答案为:
,故答案为:
 。
。
(4)C为![]() ,对应的同分异构体①能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,水解产物中含有酚羟基②分子中只有一个环状结构,故同分异构体含有
,对应的同分异构体①能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,水解产物中含有酚羟基②分子中只有一个环状结构,故同分异构体含有![]() 和-CH=CH2,两者在苯环上邻间对三种位置,其中苯环上的一氯取代产物只有两种的同分异构体的结构简式为:
和-CH=CH2,两者在苯环上邻间对三种位置,其中苯环上的一氯取代产物只有两种的同分异构体的结构简式为:![]() ,故答案为:3种;
,故答案为:3种;![]() 。
。
(5)对比CH3CHO和CH3COCOCOOH的结构简式,CH3CHO中含醛基,碳链增长,模仿题给已知I构建碳干骨架生成CH3CH=CHCHO,CH3CH=CHCHO中—CHO发生氧化反应转化为CH3CH=CHCOOH,碳碳双键与溴水发生加成反应可引入双官能团生成CH3CHBrCHBrCOOH,CH3CHBrCHBrCOOH依次发生水解反应、氧化反应即可得到目标产物;以 CH3CHO为原料制备CH3COCOCOOH的合成路线流程图为: ,故答案为:
,故答案为: 。
。

【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=+88.6 kJ·mol-1
ΔH=+88.6 kJ·mol-1
则M、N相比,较稳定的是__________。
(2)根据下列热化学方程式分析,C(s)的燃烧热△H等于_____________ (用△H1 、△H2、△H3表示)
C(s)+H2O(l)=CO(g)+H2(g); △H1
2CO(g)+O2(g)=2CO2(g); △H2
2H2(g)+O2(g)=2H2O(l); △H3
(3) 根据键能数据估算CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH=________。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
CH4的结构如图所示
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________。
(5)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) =2Al2O3(s)+3TiC(s) ΔH= -1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_____________。



