题目内容
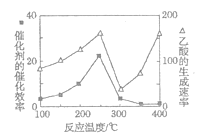
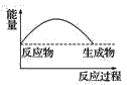
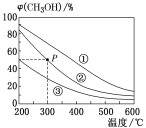
【题目】在①、②、③容积不等的恒容密闭容器中,均充入0.1molCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示。下列说法正确的是
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示。下列说法正确的是
A.该反应的正反应为吸热反应
B.三个容器的容积:①>②>③
C.在P点,CO的转化率为75%
D.在P点,向容器②中再充入CO、H2及CH3OH各0.025mol,此时υ正(CO)<υ逆(CO)
【答案】C
【解析】
A.同一容器中,升高温度,甲醇的体积分数减小,说明升高温度平衡逆向移动;
B.相同温度下,增大压强(缩小容器容积)平衡正向移动,则甲醇的体积分数增大;
C.P点,容器中甲醇的体积分数是50%,同一容器中气体的体积分数等于其物质的量分数,设此时CO的转化率为x,
该反应中 CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
开始(mol)0.1 0.2 0
反应(mol)0.1x 0.2x 0.1x
平衡(mol)0.1(1-x) 0.2(1-x) 0.1x
甲醇的体积分数=![]()
x=0.75
D.设容器体积为VL,由P点化学平衡常数与浓度商大小判断。
A.同一容器中,升高温度,甲醇的体积分数减小,说明升高温度平衡逆向移动,则正反应是放热反应,故A错误;
B.相同温度下,增大压强(缩小容器容积)平衡正向移动,甲醇的体积分数增大,由图知,甲醇的体积分数大小顺序是:①>②>③,压强大小顺序是:①>②>③,容器体积为:①<②<③,故B错误;
C.P点,容器中甲醇的体积分数是50%,同一容器中气体的体积分数等于其物质的量分数,
设此时CO的转化率为x,
该反应中 CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
开始(mol)0.1 0.2 0
反应(mol)0.1x 0.2x 0.1x
平衡(mol)0.1(1-x) 0.2(1-x) 0.1x
甲醇的体积分数=![]()
x=0.75,则CO的转化率为75%,故C正确;
D.设容器体积为VL,P点化学平衡常数K=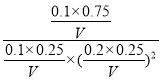 =1200V2,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时浓度商=
=1200V2,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时浓度商=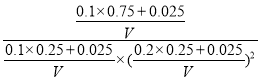 =355.6V2<K,说明平衡正向移动,则此时 υ正(CO)>υ逆(CO),故D错误;
=355.6V2<K,说明平衡正向移动,则此时 υ正(CO)>υ逆(CO),故D错误;
故选:C。