题目内容
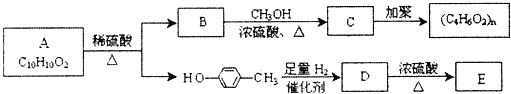
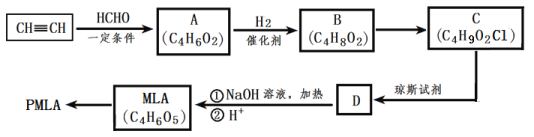
【题目】聚苹果酸(PMLA),是一种生物医学材料,可由苹果酸(MLA)经聚合反应生成。PMLA的一种合成路线如图所示。
已知:①R1-C![]() CH+
CH+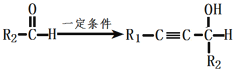
②R-CH2OH![]() R-COOH
R-COOH
(1)A中含有官能团名称为___、___。
(2)B到C的反应类型为___反应。
(3)B的核磁氢谱中有三组峰,其峰面积比为1:1:2,B的结构简式为___。
(4)D与NaOH溶液在加热条件下反应的化学方程式为___。
(5)上述转化关系中B→C和C→D这两步的顺序能否颠倒___(填“能”或“不能”),理由是___。
(6)写出与MLA具有相同官能团的所有同分异构体的结构简式___(不包含MLA)。
(7)聚酯PMLA有多种结构,写出由MLA制PMLA的化学方程式___(任写一种)。
【答案】羟基 碳碳三键 加成 HO-CH2CH=CHCH2-OH ![]() +3NaOH
+3NaOH![]() +NaCl+2H2O 不能 若先氧化则B中碳碳双键也被氧化
+NaCl+2H2O 不能 若先氧化则B中碳碳双键也被氧化 ![]() 、
、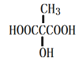 n
n +(n-1)H2O
+(n-1)H2O
【解析】
由A的分子式、结合信息,可知1分子甲醛与2分子乙炔发生加成反应生成A,则A的结构简式为HOCH2C≡CCH2OH,A与氢气发生加成反应生成B为HOCH2CH=CHCH2OH,B在一定条件下与HCl发生加成反应生成C,C为HOCH2CH2CH(Cl)CH2OH,根据已知信息②R-CH2OH![]() R-COOH,则C与琼斯试剂发生氧化反应生成D,D为HOOCCH2CH(Cl)COOH,D在氢氧化钠水溶液、加热条件下发生反应生成
R-COOH,则C与琼斯试剂发生氧化反应生成D,D为HOOCCH2CH(Cl)COOH,D在氢氧化钠水溶液、加热条件下发生反应生成![]() ,再加酸酸化制得MLA为
,再加酸酸化制得MLA为![]() ,可由苹果酸(MLA)经聚合反应生成PMLA,据此分析解答。
,可由苹果酸(MLA)经聚合反应生成PMLA,据此分析解答。
(1)A的结构简式为HOCH2C≡CCH2OH,含有官能团的名称是:羟基、碳碳三键;
(2)B为HOCH2CH=CHCH2OH,B在一定条件下与HCl发生加成反应生成C,B到C的反应类型为加成反应;
(3)B的核磁氢谱中有三组峰,其峰面积比为1:1:2,B的结构简式为HO-CH2CH=CHCH2-OH;
(4)D为HOOCCH2CH(Cl)COOH,结构中有羧基和氯原子,都可与氢氧化钠发生反应,D在氢氧化钠水溶液、加热条件下发生反应生成![]() ,化学方程式为
,化学方程式为![]() +3NaOH
+3NaOH![]() +NaCl+2H2O;
+NaCl+2H2O;
(5)C与琼斯试剂发生氧化反应生成D,B为HOCH2CH=CHCH2OH,结构中含有碳碳双键,若先发生氧化反应,则B中碳碳双键也被氧化,因此不能颠倒;
(6)MLA为![]() ,与MLA具有相同官能团的所有同分异构体的结构简式
,与MLA具有相同官能团的所有同分异构体的结构简式![]() 、
、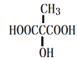 ;
;
(7)聚酯PMLA有多种结构,由MLA制PMLA发生脱水缩合反应,可以为分子内缩合,也可分子间缩合,其中一种缩合反应的化学方程式n +(n-1)H2O。
+(n-1)H2O。

 新课标阶梯阅读训练系列答案
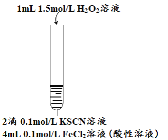
新课标阶梯阅读训练系列答案【题目】某小组在Fe2+检验实验中观察到异常现象,为探究“红色褪去”的原因,进行如下实验:
编号 | 实验I | 实验II | 实验III |
实验步骤 |
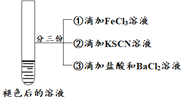
| 将实验I褪色后的溶液分三份分别进行实验
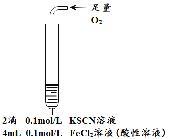
| 为进一步探究“红色褪去”的原因,又进行以下实验 ① ②取反应后的溶液,滴加盐酸和BaCl2溶液 |
现象 | 溶液先变红,片刻后红色褪去,有气体生成(经检验为O2) | ①无明显现象 ②溶液变红 ③产生白色沉淀 | ①溶液变红,一段时间后不褪色。 ②无白色沉淀产生 |
分析上述三个实验,下列叙述不正确的是
A.在此实验条件下H2O2氧化Fe2+的速率比氧化SCN-的速率快
B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化
C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与H2O2的氧化性有关
D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关