��Ŀ����
����Ŀ����ͼ��ֱ��Ǽס�������ͬѧ����Ӧ��AsO ![]() +2I��+2H+AsO
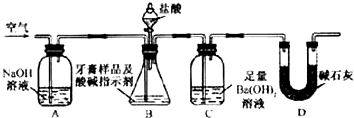
+2I��+2H+AsO ![]() +I2+H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40%NaOH��Һ��������������ȷ���ǣ� ��
+I2+H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40%NaOH��Һ��������������ȷ���ǣ� �� 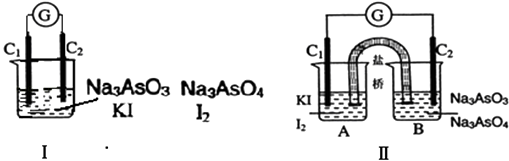
A.�������ʱ������
B.ָ�뷢��ƫת
C.�������ʱ����Һ��ɫ����
D.�������ʱ��C2������
E.�������ʱ��C1�Ϸ����ĵ缫��ӦΪI2+2e���T2I��
���𰸡�BD
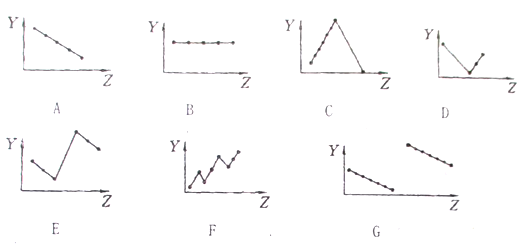
���������⣺A���������ʱ�������缫��Ϊ̼����������ԭ��ط�Ӧ����������G��ָ�벻����ƫת����A����B��������Ӧ���ɵⵥ�ʣ�����Һ��ɫ�����B��ȷ��
C���������ʱ��C2����������AsԪ��ʧȥ���ӣ���C����
D���������ʱ��C1�ϵõ����ӣ�Ϊ�����������ĵ缫��ӦΪI2+2e���T2I�� �� ��D��ȷ��
��ѡBD��
������ͼ���ձ�����μ�������Ũ���ᣬ����������ԭ��Ӧ��������ԭ��ط�Ӧ���Դ˷���A��B��
������ͼ��B�ձ�����μ�������40%NaOH��Һ����������ѧ��Ӧ������ԭ��ط�Ӧ��A�з���I2+2e���T2I�� �� Ϊ������Ӧ����B��As���ϼ����ߣ�����������Ӧ���Դ˷���C��D��

 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
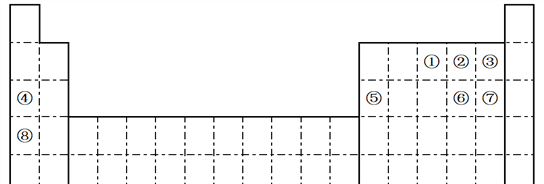
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
�� | �� | �� | ||||||
�� | �� | �� | �� | �� | �� | �� | ||
�� | �� | �� |
(1)�ڢۡ���Ԫ���У�ԭ�Ӱ뾶������___________�������ӵ�ԭ�ӽṹʾ��ͼΪ___________
(2)�١���Ԫ���У�����������Ӧ��ˮ������������ǿ����________��������ǿ����________�������Ե�����������________���������Ӧ�����ӷ���Ϊ__________��__________��__________��
(3)Ԫ�آڵ�һ��ԭ������������������1����m�˴���ԭ���γɵļ������к��еĵ�����Ϊ______________mol��
(4)�ڢ����ĵ����У���ѧ���ʽϻ��õ���___________������ʲô��ѧ��Ӧ˵������ʵ(д����Ӧ�Ļ�ѧ����ʽ)��___________________________________��