题目内容
【题目】已知:2SO2(g) + O2(g)2SO3(g) ΔH ,不同条件下反应过程能量变化如图所示。下列说法中不正确的是

A.反应的 ΔH<0
B.过程b 使用了催化剂
C.过程b 发生两步反应,第一步为吸热反应
D.使用催化剂可以降低反应活化能,提高 SO2 的平衡转化率
【答案】D
【解析】
A.根据图像可知,反应物的总能量比生成物的总能量高,则该反应是放热反应,即ΔH<0,A正确;
B.根据图像可知,过程b的活化能较低,则过程b使用了催化剂,B正确;
C.过程b分为两步反应,第一步中,中间产物的总能量比反应物的总能量高,说明第一步为吸热反应,C正确;
D. 使用催化剂可以降低反应活化能, 加快反应速率,但对于正逆反应速率都同等程度的增加,故使用催化剂不会引起平衡的移动,不能提高SO2的平衡转化率,D错误;
故选D。

 阅读快车系列答案
阅读快车系列答案【题目】![]() 、
、![]() 、
、![]() 、
、![]() 四种元素,前三种元素的简单离子都和氖原子具有相同的核外电子排布。
四种元素,前三种元素的简单离子都和氖原子具有相同的核外电子排布。![]() 元素没有正化合价;
元素没有正化合价;![]() 的氢化物的分子式为
的氢化物的分子式为![]() ,
,![]() 的
的![]() 的单质能从足量酸溶液中置换出
的单质能从足量酸溶液中置换出![]() (标准状况);
(标准状况);![]() 的原子核中没有中子。
的原子核中没有中子。
(1)根据以上条件,推断![]() 、
、![]() 、
、![]() 、
、![]() 的元素名称。
的元素名称。
A________,B ________,C ________,D ________。
(2)用电子式表示![]() 与
与![]() 、
、![]() 与
与![]() 、
、![]() 与
与![]() 相互结合成的化合物,指出其化合物的类型及所含化学键类型。
相互结合成的化合物,指出其化合物的类型及所含化学键类型。
化合物 | 电子式 | 化合物类型 | 化学键类型 |
| _____ | _____ | _____ |
| _____ | _____ | _____ |
B+D | ____ | _____ | _____ |
(3)写出![]() 与
与![]() 所形成的化合物和
所形成的化合物和![]() 与
与![]() 所形成的化合物反应的离子方程式:_______。
所形成的化合物反应的离子方程式:_______。
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据(已知![]() 为阿伏伽德罗常数的值):
为阿伏伽德罗常数的值):
试管中所加试剂及其用量/mL | 溶液退至无色所需时间/min | |||||
实验编号 | 实验温度/℃ | 0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/LKMnO4溶液 | |
① | 25 | 3.0 | v1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | v2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式:___,当该反应以实验①中数据反应完全时转移电子数为_____![]() 。
。
(2)实验①②是探究浓度对反应速率的影响,实验②③时探究温度对反应速率的影响,则表中V1=_______,V2=__________。
(3)根据实验①、②的数据,可以得到的结论是____。
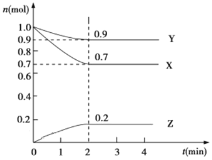
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。

该小组同学根据上述信息提出了新的假设,并设计一下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/ml | 再加入某种固体 | 溶液退至无色所需时间/min | |||
0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/L KMnO4 溶液 | ||||
④ | 25 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
①该小组同学提出的新假设是__________。
②若该小组同学提出的假设成立,应观察到__________(填实验现象)。