题目内容
【题目】某化合物的化学式为NH5,该化合物中各原子最外层都达到稀有气体的稳定结构。下列有关说法错误的是
A. 1molNH5中含有5NA个N-H键
B. NH5中既含有共价键,又含有离子键,是离子化合物
C. NH5的熔、沸点高于NH3
D. NH5固体投入少量水中可产生两种气体
【答案】A
【解析】某化合物的化学式为NH5,该化合物中各原子最外层都达到稀有气体的稳定结构,所以应该是离子化合物氢化铵:NH4H,电子式为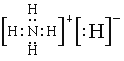 。A. 1molNH5中含有4NA个N-H键,A错误;B. NH5中既含有共价键,又含有离子键,是离子化合物,B正确;C. NH5是离子化合物,熔、沸点高于NH3,C正确;D. NH5固体投入少量水中生成氢气和一水合氨,一水合氨分解生成氨气,可产生两种气体,D正确,答案选A。
。A. 1molNH5中含有4NA个N-H键,A错误;B. NH5中既含有共价键,又含有离子键,是离子化合物,B正确;C. NH5是离子化合物,熔、沸点高于NH3,C正确;D. NH5固体投入少量水中生成氢气和一水合氨,一水合氨分解生成氨气,可产生两种气体,D正确,答案选A。

【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,气体发生装置略去)。试回答:

(1)上述反应中生成二氧化硫的化学方程式为___________________。
(2)乙同学认为还可能产生氢气的理由是______________。
(3)A中加入的试剂可能是________,作用是________;B中加入的试剂可能是_________ ,作用是________;
(4)可以证明气体X中含有氢气的实验现象是:C中:________,D中:__________。
II.该小组同学将收集的SO2气体通入0.1mol/L的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
该小组设计实验验证了假设一,
(5)请在下表空白处填写相关实验现象
实验步骤 | 实验现象 | 结论 |
实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | ___________________ | 假设一成立 |
实验2:在盛有不含O2的 25ml0.1mol/LLBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | ___________________ |
(6)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图,实验1中溶液pH变小的原因是(用离子方程式表示)___________________。