题目内容
【题目】现有温度相同、pH=a和pH=b的两种NaOH溶液,已知b=a+2,将两种溶液等体积混合后,所得溶液的pH接近于
A.a-lg2 B.b-lg2 C.a+lg2 D.b+lg2
【答案】B
【解析】
试题分析:设两溶液体积的体积都为VL,pH=a的氢氧化钠溶液中氢氧根离子浓度为:c(OH-)=10pH-14mol/L=10a-14mol/L,pH=b的氢氧化钠溶液中氢氧根离子浓度为:c(OH-)=10pH-14mol/L=10b-14mol/L=10(a+2)-14mol/L=10a-12mol/L,混合液中氢氧根离子的物质的量为:10a-14mol/L×VL+10a-12mol/L×VL(10a-14+10a-12)Vmol≈10a-12Vmol,混合液中氢氧根离子浓度为:c(OH-)=![]() =
=![]() mol/L≈
mol/L≈![]() mol/L,混合液中氢离子浓度为:c(H+)=
mol/L,混合液中氢离子浓度为:c(H+)= mol/L=2×10-a-2mol/L,混合液的pH=-lgc(H+)=-lg2×10-a-2=a+2-lg2=b-lg2,故选B。
mol/L=2×10-a-2mol/L,混合液的pH=-lgc(H+)=-lg2×10-a-2=a+2-lg2=b-lg2,故选B。

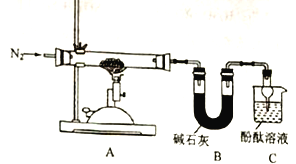
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2,在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,
(1)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显________性,用化学平衡原理解释:__________________。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________。
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
C.c(Na+)+c(H-)=c(SO32-)+c(HSO3-)+c(OH-)
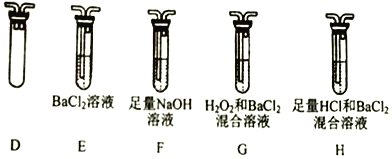
(2) 能证明Na2SO3溶液中存在SO32-+H2O![]() HSO3-+OH-水解平衡的事实是________(填序号)。
HSO3-+OH-水解平衡的事实是________(填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色褪去
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去