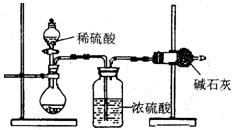
题目内容
为测定碳酸钠的质量分数(设含杂质碳酸氢钠),某学生设计了如下两个实验方案,请回答每个方案中的问题。
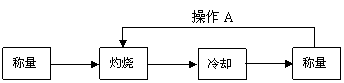 [方案Ⅰ] 重量法:
[方案Ⅰ] 重量法:
|
|||
|
(1)称量所需要的仪器是 。
(2)样品放在 仪器中灼烧。
a.蒸发皿 b.烧杯 c.坩埚
(3)实验中操作A的名称为 。
(4)如果灼烧后的样品放在空气中冷却,会造成实验结果 (填“偏大”、“偏小”或“不变”)。
(5)样品碳酸钠的质量分数 。已知该样品碳酸钠的质量分数为0.913,则本次实验的相对误差为 。
[方案II] 滴定法:①称取样品 M g;②用amol/L 过量盐酸VmL在烧杯中溶解样品,并加水稀释配成100mL溶液;③取溶解后的溶液20.00mL,用bmol/L NaOH溶液滴定,恰好用去V,mL;④重复③的操作2~3次。
(6)配成上述溶液所需要的容器的名称是 。滴定中还需要的试剂是 。
(7)操作④的目的是 。
(8)滴定测得的过量盐酸中含HCl的总物质的量的表达式为 。
(9)下列操作会使过量盐酸中含HCl测定值偏小的是 。
a.盛放氢氧化钠的滴定管只用蒸馏水洗涤
b.滴定过程中有液体溅出
c.滴定中用蒸馏水冲洗锥形瓶内壁
(10)综上所述,你认为2个方案中,较好的方案是 。
(1)电子天平 (2)c (3)恒重 (4)偏大 (5)0.892 -2.3%
(6) 100mL容量瓶 酚酞(甲基橙)
(7)多次试验取平均值,减少偶然误差
(8)bV,/200 (9)b (10)方案Ⅱ

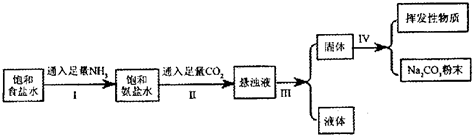
在常温下,有关物质的溶解度为:
| 物质 | NH4Cl | NaHCO3 | Na2CO3 | NaCl |
| 溶解度/g | 37.2 | 9.6 | 21.5 | 36.0 |
(2)操作I和操作II总反应的离子方程式为
(3)操作I和II不能颠倒的原因
(4)检验所得的碳酸钠粉末是否含有NaHCO3,的实验方案是(写出操作步骤、现象、结论):
(5)为了测定所制取产物的纯度(假设杂质只有碳酸氢钠).该小组的实验步骤为:
i.使用下列装置组装实验装置,并检查气密性;
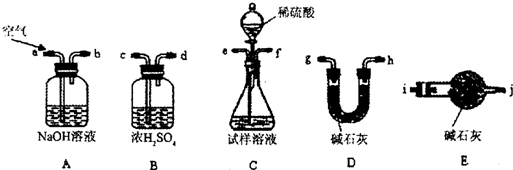
ii.称取Wg产品放入C装置的锥形瓶中,加适量蒸馏水溶解
iii.称量D装置的质量为W1g
iv.从分液漏斗滴入稀硫酸,直到不再产生气体为止
v.从a处缓缓鼓入一定量的空气,再次称量D装置质量为W2g.
vi.重复步骤v的操作,直到D装置的质量不再改变,称得D装置的质量为W3g.
根据上述实验回答如下问题:
①第i步,使用上述装置连接的接口顺序为:(b)→(e)(f)→
②产物中碳酸钠的质量分数为(数字可不必化简)
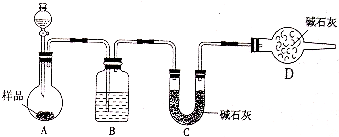
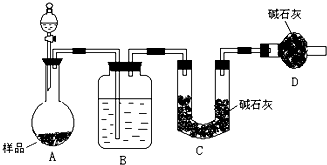 某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.
某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.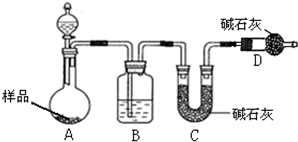 为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:
为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案: