题目内容
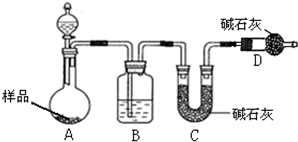 为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:
为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:(1)方案一:按如图装置进行实验,并回答以下问题.
①实验前先
②实验中除称量样品质量外,还需称
③据此实验得到的数据,结果有误差.因为实验装置还存在一个明显缺陷,该缺陷是
(2)方案二:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算.
①过滤操作中,除了烧杯外还用到的玻璃仪器有
②如加入试剂改为氢氧化钡,已知称得样品19.0g,干燥的沉淀质量为39.4g,则样品中碳酸钠的质量分数为
(3)方案三:除以上两方案以外,请你再设计一种简单方案来测定样品中碳酸钠的质量分数.
分析:(1)①制备气体实验,实验前应先检验装置气密性;盐酸具有挥发性,会影响实验结果;D干燥管中的碱石灰吸收空气中的水蒸气、二氧化碳,防止进入装置C影响测定结果;
②需要根据C装置的质量差计算出生成的二氧化碳的质量;
③装置中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差;
(2)①根据过滤操作使用的仪器完成;
②根据沉淀碳酸钡的质量计算出碳酸钡的物质的量,然后设出碳酸钠、碳酸氢钠的物质的量,根据碳酸钡的物质的量和样品质量列式计算即可;
(3)可以通过将样品充分加热,利用反应前后的质量差计算出碳酸氢钠的质量,再计算出碳酸钠的质量.
②需要根据C装置的质量差计算出生成的二氧化碳的质量;
③装置中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差;
(2)①根据过滤操作使用的仪器完成;
②根据沉淀碳酸钡的质量计算出碳酸钡的物质的量,然后设出碳酸钠、碳酸氢钠的物质的量,根据碳酸钡的物质的量和样品质量列式计算即可;
(3)可以通过将样品充分加热,利用反应前后的质量差计算出碳酸氢钠的质量,再计算出碳酸钠的质量.
解答:解:(1)①实验前,需要检查图示装置中的气密性是否良好;由于盐酸具有挥发性,影响测定结果,所以选用硫酸;为了避免空气中水分和二氧化碳进入C装置,影响测定结果,所以用D装置吸收空气中的二氧化碳和水,
故答案为:检查装置的气密性;硫酸; 防止空气中水蒸气、二氧化碳进入C管被吸收;
②知道了样品的质量,还需要测量出样品与稀硫酸反应生成的二氧化碳的质量,图中利用装置C吸收二氧化碳,所以需要称量C装置的反应前后质量,
故答案为:C;
③由于装置A和装置B中存有的二氧化碳没有完全被排出,导致反应生成的二氧化碳没有被装置C完全吸收,影响了测定结果,
故答案为:A、B中残留的CO2未全部被C吸收;
(2)①过滤操作中,除了烧杯外还用到漏斗、玻璃棒,
故答案为:玻璃棒、漏斗;
②此时发生如下反应Na2CO3+BaCl2═BaCO3↓+2NaCl,而NaHCO3与BaCl2则不反应,产生BaCO3沉淀;样品19.0g,干燥的沉淀质量为39.4g,沉淀为碳酸钡沉淀,物质的量为
=0.2mol,设碳酸钠的物质的量为xmol,碳酸氢钠的物质的量为ymol,
则:106x+84y=19.0,x+y=0.2mol,
解得:x=0.1mol,y=0.1mol,
碳酸钠物质的量为0.1mol,所以碳酸钠质量分数为
×100%≈56%,
故答案为:56%;
(3)还可以加热样品,使碳酸氢钠完全分解,利用反应前后固体的质量差计算出碳酸氢钠的质量,再计算出碳酸氢钠的质量分数,方法为:称取一定量样品充分加热后,再称取残留物的质量,计算可得样品中碳酸钠的质量分数,
故答案为:称取一定量样品充分加热后,再称取残留物的质量,计算可得样品中碳酸钠的质量分数.
故答案为:检查装置的气密性;硫酸; 防止空气中水蒸气、二氧化碳进入C管被吸收;
②知道了样品的质量,还需要测量出样品与稀硫酸反应生成的二氧化碳的质量,图中利用装置C吸收二氧化碳,所以需要称量C装置的反应前后质量,
故答案为:C;
③由于装置A和装置B中存有的二氧化碳没有完全被排出,导致反应生成的二氧化碳没有被装置C完全吸收,影响了测定结果,
故答案为:A、B中残留的CO2未全部被C吸收;
(2)①过滤操作中,除了烧杯外还用到漏斗、玻璃棒,
故答案为:玻璃棒、漏斗;
②此时发生如下反应Na2CO3+BaCl2═BaCO3↓+2NaCl,而NaHCO3与BaCl2则不反应,产生BaCO3沉淀;样品19.0g,干燥的沉淀质量为39.4g,沉淀为碳酸钡沉淀,物质的量为
| 39.4g |
| 197g/mol |
则:106x+84y=19.0,x+y=0.2mol,
解得:x=0.1mol,y=0.1mol,
碳酸钠物质的量为0.1mol,所以碳酸钠质量分数为
| 0.1mol×106g/mol |
| 19.0g |
故答案为:56%;
(3)还可以加热样品,使碳酸氢钠完全分解,利用反应前后固体的质量差计算出碳酸氢钠的质量,再计算出碳酸氢钠的质量分数,方法为:称取一定量样品充分加热后,再称取残留物的质量,计算可得样品中碳酸钠的质量分数,
故答案为:称取一定量样品充分加热后,再称取残留物的质量,计算可得样品中碳酸钠的质量分数.
点评:本题以实验探究“测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数”为载体,考查学生对于实验原理与装置理解评价、实验基本操作、化学计算等,难度中等,题目涉及到的小苏打和纯碱的化学知识是多方面的,构成了一道多角度的探究题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题: H++HA- HA-
H++HA- HA- H++A2-
H++A2- 某中学研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的性质、制法和用途,进行了如下实验:
某中学研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的性质、制法和用途,进行了如下实验: