题目内容
温度为500℃时,反应4NH3+5O2 4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为( )
4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为( )
 4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为( )
4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为( )| A.v(NO)=0.08mol/(L?s) | B.v(O2)=0.01mol/(L?s) |
| C.v(NH3)=0.002mol/(L?s) | D.v(H2O)=0.004mol/(L?s) |
C
试题分析:反应速率通常用单位时间内浓度的变化量来表示,则根据半分钟后NO的物质的量增加了0.3mol可知,NO的反应速率是
 =0.002mol/(L?s)。又因为反应速率之比是相应的化学计量数之比,所以氨气、氧气和水蒸气的反应速率分别是0.002mol/(L?s)、0.002mol/(L?s)、0.0025mol/(L?s)、0.003mol/(L?s),答案选C。
=0.002mol/(L?s)。又因为反应速率之比是相应的化学计量数之比,所以氨气、氧气和水蒸气的反应速率分别是0.002mol/(L?s)、0.002mol/(L?s)、0.0025mol/(L?s)、0.003mol/(L?s),答案选C。点评:该题是高考中的常见考点,属于中等难度的试题。该题的关键是明确反应速率的计算依据,以及反应速率与化学计量数的关系,然后结合题意和方程式灵活运用即可。

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
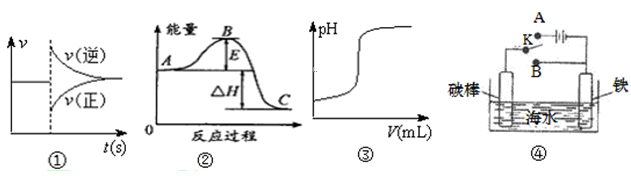
 2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是:
2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是: 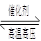 2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率( )
2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率( )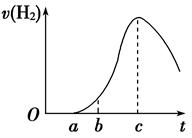
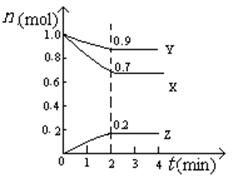
 2AB(g)的△H<0,下列说法正确的是
2AB(g)的△H<0,下列说法正确的是