题目内容
【题目】I.氢化钠(NaH) 是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。根据信息完成下列各空:
(1)氢化钠的电子式为_____________________________。
(2)氢化钠与水反应的化学方程式为_____________________,反应的氧化剂为___________。该反应过程中,被破坏的化学键有_____________(填序号,下同),形成的化学键有______________。
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系: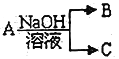 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。
(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为________________________________________________;
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为_____________________________;A 最高价氧化物的水化物与NaOH 溶液反应的离子方程式为______________________________。
【答案】 ![]() NaH+H2O=NaOH+H2↑ 水(或H2O) ①② ③ 2C+SiO2
NaH+H2O=NaOH+H2↑ 水(或H2O) ①② ③ 2C+SiO2![]() 2CO↑+Si 2Al+2OH-+2H2O=2AlO2-+3H2↑ Al(OH)3+OH-=AlO2-+2H2O
2CO↑+Si 2Al+2OH-+2H2O=2AlO2-+3H2↑ Al(OH)3+OH-=AlO2-+2H2O
【解析】I.(1)NaH是由钠离子和氢负离子组成,为离子化合物,两种离子最外层均达到8电子和2电子稳定结构,电子式为![]() ;正确答案:
;正确答案:![]() 。
。
(2)氢化钠与水反应生成氢氧化钠和氢气,化学方程式为NaH+H2O=NaOH+H2↑;NaH中H由-1价升高到0价,发生氧化反应,做还原剂;H2O中H由+1价降低到0价,发生还原反应,做氧化剂;NaH中的离子键破坏,H2O中的极性共价键被破坏;①②正确;反应生成了NaOH,形成了钠离子与氢氧根离子之间的离子键和氢原子与氧原子间的极性共价键,氢气分子中的非极性共价键;③正确;正确答案:水(或H2O);①②; ③。
II.(1)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则A是硅,工业制取单质硅的化学方程式为2C+SiO2![]() 2CO↑+Si;正确答案:2C+SiO2
2CO↑+Si;正确答案:2C+SiO2![]() 2CO↑+Si。
2CO↑+Si。
(2)若A为金属,C为气体,则A是铝,铝与NaOH溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑ ; 铝的最高价氧化物的水化物氢氧化铝与NaOH溶液反应的生成偏铝酸钠和水,离子方程式为Al(OH)3+OH-=AlO2-+2H2O;正确答案:2Al+2OH-+2H2O=2AlO2-+3H2↑;Al(OH)3+OH-=AlO2-+2H2O。

【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A. 4s时c(B)为0.78 mol/L
B. 该反应AH>0
C. 830℃达平衡时,A的转化率为20%
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为2.5
A(g)+B(g)的平衡常数为2.5