题目内容
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
(1)已知H2(g)和C(s)的燃烧热分别是285.8kJmol﹣1、393.5kJmol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是(选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将(填“变大”、“变小”或“不变”,下同),混合气体的平均式量将;
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池的负极反应式为;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,装置如图所示:请写出电解过程中Y电极附近观察到的现象;当燃料电池消耗2.8LO2(标准状况下)时,计算此时:NaCl溶液的pH=(假设溶液的体积不变,气体全部从溶液中逸出).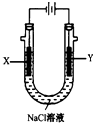
【答案】
(1)△H=﹣378.8kJ/mol
(2)ad;变小;变小
(3)CH3OCH3+16OH﹣12e﹣=2CO2﹣3+11H2O
(4)Y电极附近溶液中有气体产生,上部分呈黄绿色;14
【解析】解:(1)甲醚的燃烧热为1455kJ/mol,则燃烧方式的热化学方程式为:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;H2(g)和C(s)的燃烧热分别是285.8kJmol﹣1、393.5kJmol﹣1;热化学方程式①H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8KJ/mol;②C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/mol;③CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;依据盖斯定律计算①×3+②×2﹣③得到反应热化学方程式为:2C(s)+3H2(g)+
O2(g)=H2O(l)△H=﹣285.8KJ/mol;②C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/mol;③CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;依据盖斯定律计算①×3+②×2﹣③得到反应热化学方程式为:2C(s)+3H2(g)+ ![]() O2(g)═CH2OCH3(g):△H=﹣169.4kJ/mol;4C(s)+6H2(g)+O2(g)═2CH2OCH3(g):△H=﹣338.8kJ/mol;所以答案是:△H=﹣378.8kJ/mol;(2)①a、在反应达平衡前,c(H2)与c(H2O)的比值在变小,故当c(H2)与c(H2O)的比值保持不变时,反应达平衡,故a选;b、单位时间内有2mol H2消耗时一定会有1mol H2O生成,故不能作为平衡的标志,故b不选;c、本反应的反应物和生成物全是气体,根据质量守恒可知,在反应过程中气体的质量一直不变,而又是恒容的容器,即气体体积不变,故气体密度ρ=
O2(g)═CH2OCH3(g):△H=﹣169.4kJ/mol;4C(s)+6H2(g)+O2(g)═2CH2OCH3(g):△H=﹣338.8kJ/mol;所以答案是:△H=﹣378.8kJ/mol;(2)①a、在反应达平衡前,c(H2)与c(H2O)的比值在变小,故当c(H2)与c(H2O)的比值保持不变时,反应达平衡,故a选;b、单位时间内有2mol H2消耗时一定会有1mol H2O生成,故不能作为平衡的标志,故b不选;c、本反应的反应物和生成物全是气体,根据质量守恒可知,在反应过程中气体的质量一直不变,而又是恒容的容器,即气体体积不变,故气体密度ρ= ![]() 直不变,故密度不变不能作为平衡的标志,故c不选;d、此反应是个气体的物质的量有改变的反应,即在平衡之前,容器中气体的物质的量和压强在变化,故当压强不变时,说明反应达平衡,故d选.故选ad;②反应放热,故升高温度,平衡左移,故CH3OCH3的产率将变小;本反应的反应物和生成物全是气体,根据质量守恒可知,在反应过程中气体的质量m一直不变,而升温后平衡左移,气体的物质的量变大,故混合气体的平均式量M=
直不变,故密度不变不能作为平衡的标志,故c不选;d、此反应是个气体的物质的量有改变的反应,即在平衡之前,容器中气体的物质的量和压强在变化,故当压强不变时,说明反应达平衡,故d选.故选ad;②反应放热,故升高温度,平衡左移,故CH3OCH3的产率将变小;本反应的反应物和生成物全是气体,根据质量守恒可知,在反应过程中气体的质量m一直不变,而升温后平衡左移,气体的物质的量变大,故混合气体的平均式量M= ![]() 变小,所以答案是:变小;变小;(3)原电池负极发生氧化反应,甲醚在负极放电,碱性条件下生成碳酸根与水,电极反应式为:CH3OCH3+16OH﹣﹣12e﹣=2CO32﹣+11H2O;所以答案是:CH3OCH3+16OH﹣12e﹣=2CO2﹣3+11H2O,(4)电解池中Y电极为阳极,溶液中氯离子失电子发生氧化反应生成氯气,现象是冒气泡,上部溶液呈黄绿色,当燃料电池消耗2.8LO2(标准状况下)物质的量=
变小,所以答案是:变小;变小;(3)原电池负极发生氧化反应,甲醚在负极放电,碱性条件下生成碳酸根与水,电极反应式为:CH3OCH3+16OH﹣﹣12e﹣=2CO32﹣+11H2O;所以答案是:CH3OCH3+16OH﹣12e﹣=2CO2﹣3+11H2O,(4)电解池中Y电极为阳极,溶液中氯离子失电子发生氧化反应生成氯气,现象是冒气泡,上部溶液呈黄绿色,当燃料电池消耗2.8LO2(标准状况下)物质的量= ![]() =0.125mol,电极反应为O2+2H2O+4e﹣=4OH﹣ , 电子转移为0.5mol,电解池中 阳极电极反应为4OH﹣﹣4e﹣=2H2O+O2↑,依据电子守恒溶液中减少氢氧根离子物质的量和增加的氢离子物质的量守恒,则溶液中氢离子浓度=
=0.125mol,电极反应为O2+2H2O+4e﹣=4OH﹣ , 电子转移为0.5mol,电解池中 阳极电极反应为4OH﹣﹣4e﹣=2H2O+O2↑,依据电子守恒溶液中减少氢氧根离子物质的量和增加的氢离子物质的量守恒,则溶液中氢离子浓度= ![]() =1mol/L,此时NaCl溶液的pH=14;所以答案是:Y电极附近溶液中有气体产生,上部分呈黄绿色;14.
=1mol/L,此时NaCl溶液的pH=14;所以答案是:Y电极附近溶液中有气体产生,上部分呈黄绿色;14.
【考点精析】本题主要考查了反应热和焓变和化学平衡移动原理以及影响因素的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热;影响因素:①浓度:增大反应物(或减小生成物)浓度,平衡向正反应方向移动;②压强:增大压强平衡向气体体积减小的方向移动.减小压强平衡向气体体积增大的方向移动;③温度:升高温度,平衡向吸热反应方向移动.降低温度,平衡向放热反应方向移动;④催化剂:不能影响平衡移动才能正确解答此题.