题目内容
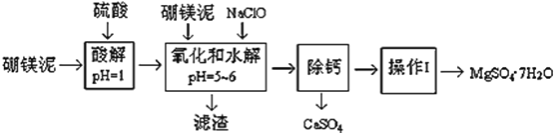
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%,质量分数),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO47H2O的工艺流程如下:
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,量取浓硫酸需要使用量筒的规格为__________(填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有__________________。
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法___________________。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤_____________________________。“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,______,便得到了MgSO47H2O .
【答案】D 2Fe2+ + ClO + 2H+ = 2Fe3+ + Cl + H2O SiO2,MnO2 取最后一滴滤液,向其中加入硫氰化钾溶液,如果溶液颜色不变红色,说明滤液中Fe3+被除尽;若出现红色,说明没有除尽 蒸发浓缩(高温浓缩),趁热过滤 过滤 或 过滤洗涤
【解析】
根据题意可知“酸解”时发生的反应:CaO+H2SO4=CaSO4+H2O,MnO+H2SO4=MnSO4+H2O,Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,FeO+H2SO4=FeSO4+H2O,Al2O3+3H2SO4=Al2(SO4)3+3H2O,SiO2既不溶解于硫酸也不被NaClO氧化,NaClO具有强氧化性,能将Fe2+和Mn2+分别氧化生成Fe3+和不溶于水的MnO2,通过水解反应将Al3+和Fe3+转化为Al(OH)3和Fe(OH)3沉淀而除去,除钙后所得滤液即为纯净的MgSO4溶液,最后通过蒸发浓缩、降温结晶得到MgSO47H2O。
(1)实验中应选取的容量瓶规格为1000mL,据此计算所需浓硫酸的体积,根据“大而近”的原则选用合适的量筒。
(2)根据硼镁泥的成分可知,还有一种具有还原性的离子应是Fe2+,反应中Fe2+被氧化为Fe3+,ClO-被还原为Cl-,据此写离子方程式。
(3)硼镁泥的成分中能够溶解于硫酸的有CaO、MnO、Fe2O3、FeO、Al2O3,只有SiO2既不溶于硫酸也不能被NaClO氧化,滤渣中应有SiO2,另外,根据题意知Mn2+被NaClO氧化为MnO2,且MnO2不溶于水,滤渣中还应有MnO2。
(4)溶液中Fe3+的检验通常使用KSCN溶液,观察溶液是否变红。
(5)由表格中溶解度数据可知,CaSO4溶解度比MgSO4小得多,MgSO4的溶解度随温度的升高而增大,CaSO4的溶解度随温度的升高而减小,所以分离MgSO4和CaSO4混合溶液,先将溶液蒸发浓缩,CaSO4析出,再趁热过滤除去滤渣,滤液为MgSO4溶液。最后将滤液蒸发浓缩、冷却结晶,过滤洗涤即可得到MgSO47H2O。
A.实验中应使用1000mL容量瓶,设需用浓硫酸VmL,根据稀释定律,![]() =1mol/L×1L,解得V=54.3mL。根据“大而近”的原则应选用100mL量筒,答案选D。
=1mol/L×1L,解得V=54.3mL。根据“大而近”的原则应选用100mL量筒,答案选D。
(2)根据硼镁泥的成分可知,还有一种具有还原性的离子应是Fe2+,反应中Fe2+被氧化为Fe3+,ClO-被还原为Cl-,因此其离子反应方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O。
(3)根据硼镁泥的成分,只有SiO2既不溶于硫酸也不能被NaClO氧化,滤渣中应有SiO2。另外,经过“酸解”与“氧化和水解”步骤,铝元素转化为Al(OH)3沉淀,铁元素全部转化为Fe(OH)3沉淀,锰元素转化为MnO2沉淀,所以滤渣中还应有SiO2和MnO2。
(4)溶液中Fe3+通常用KSCN溶液,检验方法是:取最后一滴滤液,向其中加入硫氰化钾溶液,如果溶液颜色不变红色,说明滤液中Fe3+被除尽;若出现红色,说明没有除尽。
(5)由表格中溶解度数据可知,CaSO4溶解度比MgSO4小得多,而且MgSO4的溶解度随温度的升高而增大,CaSO4的溶解度随温度的升高而减小,所以分离MgSO4和CaSO4混合溶液,应将溶液蒸发浓缩,使CaSO4充分析出,再趁热过滤,滤渣为CaSO4,滤液为MgSO4溶液。“操作Ⅰ”是从MgSO4溶液中结晶出MgSO47H2O晶体,将滤液蒸发浓缩、冷却结晶后,再过滤洗涤即得到MgSO47H2O晶体。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】前四周期元素 R、X、Y、Z、E的原子序数依次增加,它们的结构和部分信息如下表所示:
元素代号 | 部分信息 |
R | 基态R原子核外有三个能级,每个能级上电子数相同 |
X | X的双原子单质δ键和π键数目之比为1∶2 |
Y | 短周期主族元素中,原子半径最大 |
Z | Z的最高正化合价与最低负化合价之和等于4 |
E | 基态E3+的外围电子排布式是3d5 |
回答问题:
(1)E元素在周期表中的位置是________,其基态原子中电子占据的最高能层是__________________。
(2)元素 X的氢化物M,分子内含18个电子,M的结构式为_____,每个中心原子的价层电子对数是_________________。
(3)在R、X、Z的含氧酸根离子中,互为等电子体的离子组是_________________。
(4)Z元素的两种氧化物对应的水化物中,酸性较强的________,其原因是_________________。
(5)(ZX)4在常压下,高于130℃时(ZX)4分解为相应的单质,这一变化破坏的作用力是________________;它为热色性固体,具有色温效应,低于-30℃时为淡黄色,高于100℃时为深红色.
在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_________________。
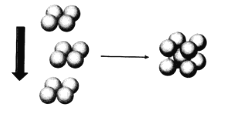
(6)常温条件下,E的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为__________,若E原子的半径为r,则单质E的原子空间利用率为________________。(列出计算式即可)
【题目】下列实验所述的变化过程与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH 溶液滴入FeSO4 溶液中 | 石蕊溶液滴入氯水中 | 向 K2Cr2O7 溶液 中滴加浓硫酸 | CO2 通入 Na2O2 |
现象 | 产生白色沉淀,最 终变为红褐色 | 溶液变红,随后迅速褪色 | 溶液黄色变浅, 橙色加深 | 固体逐渐变白 |
A. A B. B C. C D. D